Hochregulierung von PSMA: Wie antihormonelle Therapie die Radioligandentherapie unterstützt
Die PSMA-gerichtete Radioligandentherapie (RLT) — unter Verwendung von Isotopen wie Lutetium-177, Actinium-225 oder Terbium-161 — hat eine beeindruckende Wirksamkeit bei der Behandlung von Prostatakrebs gezeigt und weist ein günstiges Sicherheitsprofil auf. Ihr Erfolg hat zu einer früheren Integration in Behandlungsprotokolle geführt.
Dennoch zeigt ein gewisser Anteil der Prostatakrebszellen, insbesondere bei stark vorbehandelten Patienten, eine unzureichende PSMA-Expression, was sie auf Grundlage aktueller Bildgebung und Biomarker-Grenzwerte für eine RLT ungeeignet macht.
Die gute Nachricht ist jedoch: Eine niedrige PSMA-Expression ist nicht unbedingt ein Endpunkt. Sie kann pharmakologisch hochreguliert werden — und damit den Weg ebnen, dass auch diese Patienten von der RLT profitieren können. Schauen wir uns das genauer an.
Was reguliert PSMA?
In normalem (gutartigem) Prostatagewebe ist die PSMA-Expression niedrig. Trotz seines irreführenden Namens (Prostataspezifisches Membranantigen) ist es weder wirklich prostataspezifisch noch besonders häufig in Prostatazellen vorhanden. Der Name entstand lediglich, weil PSMA zuerst auf der Oberfläche von Prostatazellen entdeckt wurde; die korrekte Bezeichnung lautet Folat-Hydrolase.
Das Androgenrezeptor-(AR)-Signal — also wenn männliche Hormone (Androgene) wie Testosteron oder Dihydrotestosteron (DHT) an Androgenrezeptoren auf Zelloberflächen, insbesondere in der Prostata, binden — unterdrückt die PSMA-Expression, indem es das FOLH1-Gen herunterreguliert.
Was in die eine Richtung wirkt, wirkt auch umgekehrt: Wenn Testosteron fehlt (durch medikamentöse Unterdrückung oder Blockade des Androgenrezeptors), wird das FOLH1-Gen — einschließlich seiner Androgen-Bindestelle — hochreguliert, was zu einer (vorübergehenden) Überexpression von PSMA führt. Dieser Effekt ist am ausgeprägtesten in Zellen mit zunächst niedriger PSMA-Expression, wie präklinische Experimente gezeigt haben. (Impact of Androgen Receptor Activity on Prostate-Specific Membrane Antigen Expression in Prostate Cancer Cells - PubMed.)
Prostatakrebs, AR-Signalgebung und PSMA: ein komplexes Wechselspiel
Hormonempfindlicher Prostatakrebs ist für das Überleben und die Vermehrung der Tumore auf die AR-Signalgebung angewiesen. Daher ist eine der First-Line-Therapien, diesen Signalweg zu unterbrechen – entweder durch:
- Absenken des Testosteronspiegels (z.B. mit GnRH-Antagonisten wie Orgovyx) oder
- direkte Blockade des AR (z.B. mit AR-Inhibitoren wie Enzalutamid oder Apalutamid).
In diesen frühen Stadien des hormonempfindlichen Karzinoms kann die PSMA-Expression vorübergehend ansteigen, wenn eine Androgendeprivationstherapie (ADT) begonnen wird (siehe Mechanismus oben). Nach mehrwöchiger Behandlung tendiert der PSMA-Spiegel jedoch wieder zu sinken, da die meisten Zellen ohne Testosteron Apoptose (programmierten Zelltod) durchlaufen.
Leider überlebt ein Teil der Krebszellen diesen Testosteronentzug und wird als evolutionäre Reaktion auf die ADT schließlich kastrationsresistent. In diesem Stadium werden die Tumore oft wieder PSMA-avid, was sie erneut zu geeigneten Zielen für eine Radioligandentherapie macht. Dies geschieht, weil das PSMA-Gen FOLH1 ohne AR-Signalgebung überexprimiert bleibt. Somit ist die PSMA-Hochregulation im Wesentlichen ein Nebenprodukt der adaptiven Mechanismen, die es Krebszellen ermöglichen, unter Therapiedruck zu überleben. Die resistenten Zellen, die den Androgenentzug überwinden, vermehren sich und gedeihen, was die ADT letztlich unwirksam macht.
In diesen Fällen ist die Einleitung einer Therapie mit Androgenrezeptorweg-Inhibitoren (ARPI) der Standardansatz, obwohl der Nutzen begrenzt ist, da der Androgenrezeptor nicht mehr der primäre Treiber des Krebswachstums ist. Die daraus resultierende PSMA-Hochregulation bleibt jedoch bestehen – und dies schafft eine Verwundbarkeit, die wir ausnutzen können.
Ein neues Paradigma: Die Kombination von AR-Signalweg-Unterdrückung mit RLT
Genau das untersuchen aktuelle klinische Studien: die frühzeitige Identifizierung und gezielte Bekämpfung jener adaptiven Krebszellen, die eine ADT überleben, um so potenziell die Fluchtmechanismen des Tumors zu unterbrechen. Die Ergebnisse sind vielversprechend: viele Patienten zeigen kurz nach Beginn der AR-Blockade einen deutlichen Anstieg der PSMA-Expression, was einen Patienten mit "niedriger PSMA-Expression" potenziell zu einem Kandidaten für eine RLT machen könnte.
Ein aktueller Beweis für dieses Konzept in den initialen hormonsensitiven Stadien wurde auf dem ASCO 2025 präsentiert: die ersten Ergebnisse der PSMAddition-Studie, die bessere Behandlungsergebnisse für RLT plus ADT im Vergleich zu einer ADT allein demonstrierten.
Diese Synergie zwischen hormoneller Blockade und PSMA-gerichteter Therapie könnte ein neues Kapitel in der personalisierten Prostatakrebstherapie einläuten und ihren Einsatz in sehr frühe Krankheitsstadien verlagern.
Unsere klinische Erfahrung
In unserer Klinik wenden wir dieses Konzept bereits seit vielen Jahren in der Praxis an. Bei ausgewählten Patienten setzen wir erfolgreich eine initiale ADT ein, um die PSMA-Expression gezielt vor einer geplanten Radioligandtherapie zu stimulieren – mit ausgezeichneten Ergebnissen. Dieser vorbereitende Schritt kann ein entscheidender Wendepunkt für Patienten sein, die im initialen Stadienbestimmungs-PSMA-PET eine heterogene oder niedrige PSMA-Expression aufweisen.
Zusammenfassung
- Eine niedrige PSMA-Expression ist nicht irreversibel.
- Die Unterdrückung des Androgen-Signalwegs (durch Absenken des Testosteronspiegels oder den Einsatz von AR-Inhibitoren) kann eine Hochregulierung der PSMA-Expression bewirken.
- Dies eröffnet neue Möglichkeiten für eine frühzeitige RLT– selbst bei Patienten, die zunächst als ungeeignet galten.
- Die Kombination von AR-gerichteten Therapien mit PSMA-gerichteten Therapien könnte additive und möglicherweise synergistische klinische Vorteile bieten.
Da sich die Behandlungsstrategien ständig weiterentwickeln, entwickelt sich das Wechselspiel zwischen hormoneller Manipulation und molekularer nuklearmedizinischer Therapie zunehmend zu einem wirksamen Instrument im Kampf gegen Prostatakrebs.
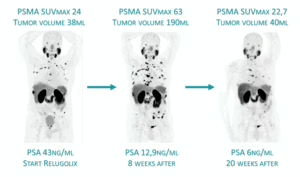
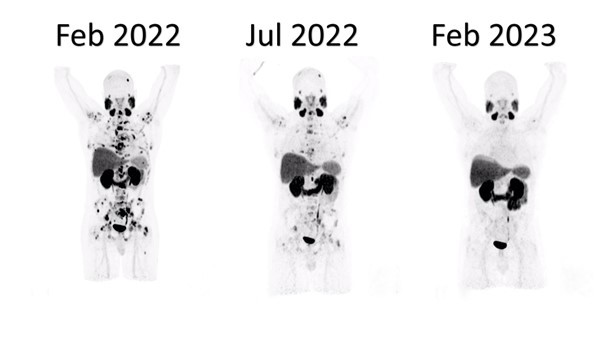
Sequenzielle PSMA-PET-Untersuchungen bei einem Patienten unter neu eingeleiteter ADT, der trotz eines signifikanten Rückgangs der PSA-Werte nach 8 Wochen eine ausgeprägte PSMA-Überexpression zeigt (PSMA-PET-Pseudoprogression des PSMA-Volumens bei echter Progression der PSMA-Aufnahme).