Einsatz von Alphastrahlern in Radiopharmazeutika für die Krebsbehandlung
Im fortwährenden Kampf gegen Krebs haben sich die Radiopharmazeutika als wirksame Waffe erwiesen, und Alphastrahler wie Actinium-225, Astatin-211 und Blei-212 gewinnen schnell an Bedeutung. Diese Alpha-emittierenden Isotope revolutionieren die Krebsbehandlung und bieten eine gezielte Therapie mit dem Potenzial, bösartige Zellen auszurotten und gleichzeitig die Schädigung des umgebenden gesunden Gewebes zu minimieren.
Alphastrahler: Ein kurzer Überblick
Alpha-Teilchen bestehen aus zwei Protonen und zwei Neutronen und sind hochenergetisch. Ihre hohe Energie und kurze Reichweite (wenige Zelldurchmesser) machen sie ideal für die präzise Zerstörung von Krebszellen. Diese Eigenschaften ermöglichen es ihnen, einen Doppelstrangbruch in der DNA zu verursachen, was den Krebszellen den Garaus bereitet, aber gleichzeitig die Kollateralschäden an benachbarten gesunden Zellen minimiert. Die Alphastrahler werden die Beta-Strahler wie Lutetium nicht verdrängen, sondern ergänzen, wie Sie unten am Beispiel von 225Ac in der Behandlung von Prostatakrebs sehen werden.
Actinium-225: Präzision in Aktion
Actinium-225 steht an der Spitze der Forschung über Alphastrahler zur Krebsbehandlung. Mit einer Halbwertszeit von ca. 10 Tage zeigten die mit Actinium-225-markierte Radioliganden eine bemerkenswerte Wirksamkeit bei der Behandlung von metastasierendem Krebs, insbesondere Prostatakarzinom. Klinische Studien haben eine signifikante Tumorreduktion und verlängerte Überlebensraten bei Patienten mit fortgeschrittenem Prostatakrebs gezeigt.
225Ac-PSMA bei der Behandlung von Prostatakrebs
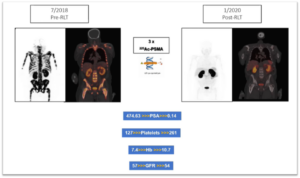
Speziell bei Knochenmarkinfiltration bei metastasiertem Prostatakrebs können Alphastrahler in perfekter Kombination mit Lutetium wirken. Die erste Sitzung der Radioligandentherapie, die mit dem stärkeren Alphastrahler (zB. 225Ac-PSMA) durchgeführt wird, ermöglicht es, Krebszellen im Knochenmark zu zerstören, ohne das Knochenmark selbst zu beschädigen. Dadurch kann der Körper seine Funktion der Hämatopoese, d.h. der Blutzellenproduktion, wiederherstellen. Die Studie in Südafrika war die erste, dies zu demonstrieren. Ein Patient mit schwerem metastasiertem Prostatakrebs und signifikanter diffuser Knocheninfiltration erholte sich nach 2 Sitzungen von 225Ac-PSMA von schwerwiegender Anämie. Die Hämoglobinwerte und die Anzahl der Blutplättchen haben sich dramatisch verbessert, was offensichtlich zur Wiederbelebung der angeborenen Immunantwort des Körpers führt.
Wir haben die etablierte Praxis, unseren Patienten mit entsprechendem Krankheitsbild eine Kombinationstherapie von 1 + 2 (ein 225Ac-PSMA + zwei 177Lu-PSMA Sitzungen) anzubieten.
225Ac-DOTATATE bei der Behandlung von NETs und Meningeomen
Die Behandlung von Prostatakrebs mit Radiopharmazeutika gilt heute aufgrund ihrer nachgewiesenen Wirksamkeit als naheliegende Therapie. Die Vielseitigkeit von Actinium-225 ermöglicht die Konjugation mit verschiedenen anderen zielenden Molekülen, wodurch seine potenziellen Anwendungen auf andere Krebsarten wie neuroendokrine Tumoren (NETs) und Meningeome ausgeweitet werden.
Die Verwendung von 177Lu-DOTATATE bei der Behandlung von NETs liegt eigentlich vor der Verwendung von 177Lu-PSMA zur Prostatakrebstherapie. Tumore können jedoch manchmal resistent gegen Strahlentherapien mit niedrigerem LET (Linear Energy Transfer), wie zB. Betastrahlern, werden. Darüber hinaus sprechen einige aggressive oder fortgeschrittene Formen möglicherweise nicht ausreichend auf Beta-emittierende Therapien an. In solchen Fällen schneiden Alpha-Strahler aufgrund ihrer höheren Zytotoxizität besser ab.
Die Entdeckung von DOTATATE-Rezeptoren in Meningeomzellen, einer weit verbreiteten Art von Hirntumor, war ein weiterer Durchbruch jüngster Zeit. Angesichts der komplexen Natur des Gehirns, wo die Tumore von den kritischen Strukturen eng umhüllt sind, wird eine präzise Tumoranpeilung mit minimaler Strahlenbelastung für gesundes Hirngewebe unerlässlich, um Nebenwirkungen zu mildern. Alphastrahler sind mit ihrer hochkonzentrierten, aber räumlich begrenzten Leistung eine ideale Wahl.
225Ac-DOTATATE ist in unserer Klinik verfügbar.
Astatin-211: Ein neuartiger Ansatz
Astatin-211 ist ein weiterer vielversprechender Alphastrahler, der sich durch seine günstige Halbwertszeit (7,2 Stunden) und starke Alpha-Emissionen auszeichnet. Seine kurze Halbwertszeit sorgt dafür, dass der radioaktive Zerfall hauptsächlich innerhalb des Tumors stattfindet, wodurch die langfristige Strahlenbelastung des Patienten minimiert wird.
Astatin-211 wird bei der Behandlung von Gliomen erforscht, eines Hirntumors mit begrenzten Behandlungsmöglichkeiten. Forscher haben mit Astatin-211 markierte monoklonale Antikörper entwickelt, die spezifisch auf tumorassoziierte Antigene abzielen. Klinische Studien in der Frühphase deuten darauf hin, dass dieser Ansatz dem Tumor eine hohe Strahlendosis zuführen und gleichzeitig normales Hirngewebe schonen kann, was Hoffnung auf bessere Ergebnisse bei Gliompatienten bietet.
Blei-212: Eine Dual-Mode-Therapie
Blei-212 zeichnet sich durch seine einzigartigen Zerfallseigenschaften aus und emittiert sowohl Alpha- als auch Beta-Teilchen. Diese Dual-Mode-Emission kann in bestimmten therapeutischen Kontexten vorteilhaft sein. Die Alpha-Partikel bieten eine hochenergetische Zytotoxizität mit kurzer Reichweite, während die Beta-Partikel eine größere Reichweite bieten und möglicherweise auf Mikrometastasen abzielen.
212Pb-DOTAMTATE hat kürzlich von der FDA den Status einer "bahnbrechenden Therapie" für die Behandlung von Patienten mit fortgeschrittenen SSTR-exprimierenden gastroenteropankreatischen neuroendokrinen Tumoren (GEP-NETs) erhalten. Diese Bezeichnung des 212Pb-DOTAMTATE, einem SSTR-zielgerichteten-Peptid, welches mit Alpha-Partikel-erzeugendem Blei-212 radioaktiv markiert ist, wird durch klinische Phase-1- und laufende Phase-2-Studien (NCT05153772) untermauert.”[2]
Blei-212 wird auch für den Einsatz bei der Behandlung von Eierstockkrebs untersucht. Die Radiopharmazeutik 212Pb-TCMC-Trastuzumab zielt auf den HER2-Rezeptor ab, der bei einigen Eierstockkrebsarten überexprimiert wird. Präklinische Studien haben gezeigt, dass dieses Compound in Tiermodellen die Tumorlast effektiv reduzieren und das Überleben verbessern kann. Klinische Studien sind im Gange, um seine Sicherheit und Wirksamkeit bei Patienten zu bewerten.
Umgang mit Toxizität
Alphastrahler bieten zwar eine präzise Zielanpeilung, aber ihre hohe Energie kann auch Risiken bergen, wenn nicht ausreichend kontrolliert. Zum Beispiel neigt bei der Behandlung von Prostatakrebs zu viel 225Ac-PSMA dazu, die Speicheldrüsen zu schädigen (sie exprimieren auch die PSMA-Enzyme genau wie die Prostatakrebszellen), was zu schwerer Xerostomie (Mundtrockenheit) führt, wobei die Nebenwirkungen den Nutzen überwiegen. Ein Zyklus mit 225Ac-PSMA zum Anfang reicht oft bereits aus, um den gewünschten Therapieeffekt zu erzielen und gleichzeitig die Speicheldrüsen zu schonen.
Die Zukunft von Alphastrahlern in der Krebstherapie
Die Zukunft der Alphastrahler in der Krebstherapie sieht vielversprechend aus, mit laufender Forschung und klinischen Studien, die den Weg für neue Behandlungsparadigmen ebnen. Die Integration fortschrittlicher bildgebender Verfahren wie PET und SPECT (z.B. bei Blei-212) ermöglicht die Echtzeitüberwachung der radiopharmazeutischen Verteilung und des therapeutischen Ansprechens. Dieses Feedback kann verwendet werden, um Behandlungspläne anzupassen und die Ergebnisse zu verbessern.
Darüber hinaus werden Ansätze der personalisierten Medizin erforscht, bei denen die spezifischen genetischen und molekularen Eigenschaften des Tumors eines Patienten genutzt werden, um die radiopharmazeutische Therapie anzupassen. Dieser präzisionsmedizinische Ansatz hat das Potenzial, die Wirksamkeit und Sicherheit von Alpha-Emitter-Therapien weiter zu verbessern.
Fazit
Alphastrahler wie Actinium-225, Astatin-211 und Blei-212 stellen einen bedeutenden Fortschritt auf dem Gebiet der Radiopharmazeutika zur Krebsbehandlung dar. Ihre Fähigkeit, Krebszellen zielgerichtete, tödliche Strahlendosen zuzuführen, bietet ein mächtiges Werkzeug im Kampf gegen bösartige Erkrankungen. Mit dem Fortschritt der Forschung und der Bewältigung von Herausforderungen versprechen diese Alpha-emittierenden Radiopharmazeutika, das Überleben und die Lebensqualität von Krebspatienten weltweit zu verbessern.
[1] [225Ac]Ac-PSMA-617 α-radioligand therapy of patients with extensive skeletal metastases of castration-resistant prostate cancer, Sathekge et al. 2022
[2] "FDA Grants Breakthrough Therapy Designation to Novel Agent in GEP-NETs"
Bibliographie:
Matthew R. Griffiths, David A. Pattison, Melissa Latter, Kevin Kuan, Stephen Taylor, William Tieu, Thomas Kryza, Danielle Meyrick, Boon Quan Lee, Aaron Hansen, Stephen E. Rose, Simon G. Puttick First-in-Human 212Pb-PSMA–Targeted α-Therapy SPECT/CT Imaging in a Patient with Metastatic Castration-Resistant Prostate Cancer Journal of Nuclear Medicine Feb 2024, jnumed.123.267189; DOI: 10.2967/jnumed.123.267189
Albertsson P, Bäck T, Bergmark K, Hallqvist A, Johansson M, Aneheim E, Lindegren S, Timperanza C, Smerud K, Palm S. Astatine-211 based radionuclide therapy: Current clinical trial landscape. Front Med (Lausanne). 2023 Jan 6;9:1076210. doi: 10.3389/fmed.2022.1076210. PMID: 36687417; PMCID: PMC9859440.
Lawal IO, Morgenstern A, Vorster M, Knoesen O, Mahapane J, Hlongwa KN, Maserumule LC, Ndlovu H, Reed JD, Popoola GO, Mokoala KMG, Mdlophane A, Bruchertseifer F, Sathekge MM. Hematologic toxicity profile and efficacy of [225Ac]Ac-PSMA-617 α-radioligand therapy of patients with extensive skeletal metastases of castration-resistant prostate cancer. Eur J Nucl Med Mol Imaging. 2022 Aug;49(10):3581-3592. doi: 10.1007/s00259-022-05778-w. Epub 2022 Apr 6. PMID: 35384462.
Metebi A, Kauffman N, Xu L, Singh SK, Nayback C, Fan J, Johnson N, Diemer J, Grimm T, Zamiara M, Zinn KR. Pb-214/Bi-214-TCMC-Trastuzumab inhibited growth of ovarian cancer in preclinical mouse models. Front Chem. 2024 Jan 25;11:1322773. doi: 10.3389/fchem.2023.1322773. PMID: 38333550; PMCID: PMC10850308.
Video “Alpha is More Than Just Ac-225: Pb-212” JNM Podcast. Ken Herrmann, MD; David Bauer, PhD, from Memorial Sloan Kettering Cancer Center; Jane Sosabowski, BSc, MSc, PhD, from Queen Mary, University of London; Nick Fletcher, PhD, from the University of Queensland, Australia.
Demirci E, Alan Selçuk N, Beydağı G, Ocak M, Toklu T, Akçay K, Kabasakal L. Initial Findings on the Use of [225Ac]Ac-DOTATATE Therapy as a Theranostic Application in Patients with Neuroendocrine Tumors. Mol Imaging Radionucl Ther. 2023 Oct 20;32(3):226-232. doi: 10.4274/mirt.galenos.2023.38258. PMID: 37870290; PMCID: PMC10600558.
Stallons TAR, Saidi A, Tworowska I, Delpassand ES, Torgue JJ. Preclinical Investigation of 212Pb-DOTAMTATE for Peptide Receptor Radionuclide Therapy in a Neuroendocrine Tumor Model. Mol Cancer Ther. 2019 May;18(5):1012-1021. doi: 10.1158/1535-7163.MCT-18-1103. Epub 2019 Mar 29. PMID: 30926632; PMCID: PMC6497546.
Sabrina Serani, February 12, 2024, FDA Grants Breakthrough Therapy Designation to Novel Agent in GEP-NETs, retrieved 03.06.2024 from https://www.targetedonc.com/view/fda-grants-breakthrough-therapy-designation-to-novel-agent-in-gep-nets