Doble golpe contra el cáncer de próstata oculto: Lutecio-177 + Terbio-161 frente a micrometástasis no detectables
Doble golpe contra el cáncer de próstata oculto: Lutecio-177 + Terbio-161 frente a micrometástasis no detectables
Los avances recientes en la terapia con radioligandos (RLT por sus siglas en inglés) dirigida a PSMA ponen de relieve su papel cada vez más importante en la erradicación de la enfermedad micrometastásica oculta en el cáncer de próstata.
Lutecio-177: ganando la batalla en fases tempranas frente a recurrencias limitadas
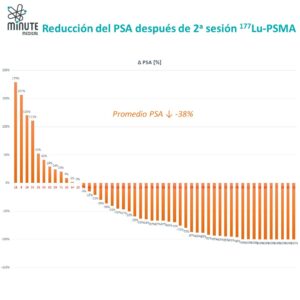
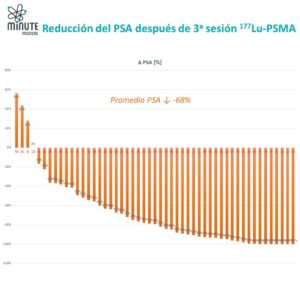
El ensayo fase II LUNAR en cáncer de próstata hormonosensible recurrente oligometastásico (solo en unos pocos sitios) demostró que añadir dos ciclos de ¹⁷⁷Lu-PNT2002 antes de la radioterapia externa de alta dosis (radioterapia corporal ablativa estereotáctica o SABR por sus siglas en inglés) dirigida a las metástasis visibles prolongó de forma significativa la supervivencia libre de progresión en comparación con SABR sola (de aproximadamente 7 meses a más de 17 meses). El tratamiento fue muy bien tolerado, con apenas efectos secundarios adicionales. Este éxito se atribuye al abordaje amplio de micrometástasis que expresan PSMA y que no son detectables mediante la diagnóstico de imagen convencional.
Terbio-161: el radionúclido de nueva generación con potencia aumentada
Partiendo de estos resultados, los datos emergentes con radioligandos PSMA marcados con ¹⁶¹Tb —procedentes de los estudios fase I/II en curso (VIOLET), así como de estudios piloto y registros en la Universidad del Sarre— muestran un efecto de la radiación superior del Terbio-161 frente al Lutecio-177. El ¹⁶¹Tb emite partículas beta de energía intermedia comparable, pero añade una abundante emisión de electrones de conversión y Auger de alta transferencia lineal de energía, lo que se traduce en dosis de radiación absorbida significativamente más altas a nivel de células individuales y en conglomerados micrometastásicos (hasta varias veces mayores a nivel del núcleo en modelos preclínicos). Esta citotoxicidad aumentada es especialmente eficaz frente a enfermedad de baja carga tumoral no detectable, y muestra respuestas prometedoras y un buen control tumoral incluso en pacientes con mCRPC fuertemente pretratados, en quienes la enfermedad progresa pese a una RLT estándar con ¹⁷⁷Lu-PSMA.
El KO 1–2: Lutecio-177 + Terbio-161
En conjunto, estos avances posicionan a la RLT dirigida a PSMA como un pilar fundamental de la terapia dirigida a micrometástasis en todos los estadios de la enfermedad, con el Terbio-161 representando una terapia de nueva generación con potencia aumentada. Un enfoque combinado inteligente en fases tempranas —como 1–2 ciclos de ¹⁷⁷Lu-PSMA seguidos de ¹⁶¹Tb-PSMA— podría utilizar Lutecio-177 para atacar los sitios tumorales más grandes, mientras se aprovecha la potencia aumentada del ¹⁶¹Tb para eliminar más eficazmente los reservorios micrometastásicos resistentes y potencialmente lograr resultados más duraderos.
En nuestra clínica aplicamos precisamente este protocolo combinado, para ofrecer a los pacientes la mejor oportunidad de tratar tanto los tumores visibles como los ocultos.
Bibliografía
Buteau JP, Kostos L, Jackson PA, Xie J, Haskali MB, Alipour R, McIntosh LE, Emmerson B, MacFarlane L, Martin CA, Chan J, Williams SE, Jewell KE, Eifer M, Hamilton AJ, Harris WQ, Akhurst T, Au L, Cardin AJ, Furic L, Kashyap RK, Kong G, Ravi Kumar AS, Murphy DG, Ravi R, Saghebi J, Sandhu S, Tran B, Azad AA, Hofman MS. First-in-human results of terbium-161 [161Tb]Tb-PSMA-I&T dual beta-Auger radioligand therapy in patients with metastatic castration-resistant prostate cancer (VIOLET): a single-centre, single-arm, phase 1/2 study. Lancet Oncol. 2025 Aug;26(8):1009-1017. doi: 10.1016/S1470-2045(25)00332-8. Epub 2025 Jul 3. PMID: 40617237.
Amar U. Kishan et al.177Lu-Prostate-Specific Membrane Antigen Neoadjuvant to Stereotactic Ablative Radiotherapy for Oligorecurrent Prostate Cancer (LUNAR): An Open-Label, Randomized, Controlled, Phase II Study. J Clin Oncol 0, JCO-25-01553 DOI:10.1200/JCO-25-01553
Rosar, F., Burgard, C., Petrescu, C., Blickle, A., Bartholomä, M., Maus, S., Bastian, M.B., Speicher, T., Schaefer-Schuler, A., Ezziddin, S. (2025). Pilot experience of [161Tb]Tb-PSMA-617 RLT in mCRPC patients after conventional PSMA RLT within a prospective registry. Theranostics, 15(17), 9019-9028. https://doi.org/10.7150/thno.115831.
“Augerlicious Terbium 161 Double Punch to Cancer Cells - Global Knowledge Exchange Webinar” ProsTIC TV
Schaefer-Schuler A, Burgard C, Blickle A, Maus S, Petrescu C, Petto S, Bartholomä M, Stemler T, Ezziddin S, Rosar F. [161Tb]Tb-PSMA-617 radioligand therapy in patients with mCRPC: preliminary dosimetry results and intra-individual head-to-head comparison to [177Lu]Lu-PSMA-617. Theranostics. 2024 Feb 24;14(5):1829-1840. doi: 10.7150/thno.92273. PMID: 38505615; PMCID: PMC10945337.
Rosar F, Maus S, Schaefer-Schuler A, Burgard C, Khreish F, Ezziddin S. New Horizons in Radioligand Therapy: 161Tb-PSMA-617 in Advanced mCRPC. Clin Nucl Med. 2023 May 1;48(5):433-434. doi: 10.1097/RLU.0000000000004589. Epub 2023 Feb 8. PMID: 36758550.
Tschan VJ, Busslinger SD, Bernhardt P, Grundler PV, Zeevaart JR, Köster U, van der Meulen NP, Schibli R, Müller C. Albumin-Binding and Conventional PSMA Ligands in Combination with 161Tb: Biodistribution, Dosimetry, and Preclinical Therapy. J Nucl Med. 2023 Oct;64(10):1625-1631. doi: 10.2967/jnumed.123.265524. Epub 2023 Jul 13. PMID: 37442604.