Рубрика: Новости
¹⁶¹Tb-ПСМА: новая надежда для пациентов с метастатическим раком предстательной железы (РПЖ)
¹⁶¹Tb-ПСМА: новая надежда для пациентов с метастатическим раком предстательной железы (РПЖ)
Исследование VIOLET – первые результаты
Совпадая с запуском этой терапии в нашем центре, обнародованы предварительные результаты исследования VIOLET – первого клинического испытания ¹⁶¹Tb-ПСМА на людях. И они весьма обнадеживающи! У 30 пациентов не было выявлено дозолимитирующей токсичности после шести циклов лечения (до 7,4 ГБк). На основании этих обнадеживающих результатов был инициирован новый этап исследования с дозой 9,5 ГБк.
Радиолигандная терапия ¹⁷⁷Lu-ПСМА доказала свою высокую эффективность при РПЖ, но у некоторых пациентов в конечном итоге наблюдается прогрессирование заболевания. Вероятная причина этому – наличие энергетически защищенных микрометастазов и единичных опухолевых клеток, которые поглощают очень мало излучения из-за своих малых размеров и ограниченной массы. Бета-частицы, испускаемые лютецием-177, имеют среднюю длину пробега ~0,7 мм (диапазон: 0,04–1,8 мм), что значительно превышает размер единичных опухолевых клеток, составляющий всего несколько микрометров (7–13 мкм). В результате большая часть излучения проходит мимо этих крошечных раковых клеток, не доставляя летальную дозу энергии и позволяя болезни прогрессировать.
В отличие от этого, тербий-161 испускает большое количество оже- и конверсионных электронов с гораздо меньшей длиной пробега (нанометры – микрометры). Это обеспечивает точное высокоэнергетическое воздействие непосредственно на единичные опухолевые клетки и микрометастазы, потенциально делая его более эффективным, чем лютеций-177, и приводя к уничтожению этих устойчивых раковых клеток. Кроме того, тербий-161 может дополнительно снизить лучевую токсичность, минимизируя воздействие на окружающие здоровые ткани.
Радиолигандная терапия ¹⁶¹Tb-ПСМА уже доступна в нашем центре.
Исследование VIOLET названо в честь покойного доктора Джона Вайолета, радиоонколога из Онкологического центра Питера МакКаллума в Мельбурне (Австралия), который проявлял большой интерес к терапии оже-электронами. Цель исследования – определить максимально переносимую дозу, профиль безопасности и противоопухолевую активность ¹⁶¹Tb-ПСМА у пациентов с мКРРПЖ (метастатическим кастрационно-резистентным раком предстательной железы). Терапия проводится в амбулаторных условиях, а ключевые задачи включают измерение поглощенных доз излучения, динамику ПСА, показатели выживаемости и качество жизни по оценке пациентов.
Интервью с профессором Хартенбахом
Интервью с профессором Хартенбахом, проведённое Primo Medico 31 марта 2025г. (аудио на немецком)
Специализированный подкаст Primo Medico с Сюзанной Амрайн — «Медицина для ушей»
При раке предстательной железы (РПЖ) точное и раннее выявление опухоли и её распространения имеет решающее значение для последующего лечения. Золотым стандартом диагностики в этом случае является ПСМА ПЭТ/КТ. Она также позволяет проводить прицельную и эффективную терапию с использованием радиомеченых лигандов. Я беседую с профессором Маркусом Хартенбахом о тесной связи между терапией и диагностикой — так называемой тераностике — а также о принципах и эффектах радиолигандной терапии. Он является специалистом по ядерной медицине и управляющим директором Minute Medical в Вене.
- [00:48] Почему ПСМА ПЭТ/КТ так важна?
- [03:40] Как работает радиолигандная ПСМА-терапия?
- [05:21] Какие радионуклиды используются?
- [08:28] Почему Вы проводите терапию амбулаторно?
- [11:03] Чем Ваш метод лечения отличается от других терапий?
- [13:00] Насколько хорошо пациенты переносят радиолигандную терапию?
- [14:42] Как Вы оцениваете эффективность лечения?
- [16:37] Можно ли повторить терапию?
PrimoMedico (PM): Профессор Хартенбах, почему ПСМА-ПЭТ/КТ играет такую важную роль в последующем лечении РПЖ?
Проф. Маркус Хартенбах (MХ): Да, уважаемая госпожа Амрайн, прежде всего большое спасибо за организацию этого подкаста и тёплый привет от Minute Medical здесь, в Вене.
ПСМА-ПЭТ/КТ по сути является входом в то, о чём Вы уже упомянули — тераностику — и в случае РПЖ это довольно специфический подход. Это означает, что мы ищем в организме очень конкретную целевую структуру. Речь идёт меньше о классической визуализации, а больше о визуализации молекулярных маркеров на поверхности клеток.
ПСМА, или простатоспецифический мембранный антиген — это название на самом деле несколько вводит в заблуждение, потому что на самом деле это фермент под названием фолат-гидролаза. Этот фермент теперь можно специфически визуализировать, и ПЭТ/КТ-сканер — это инструмент, который и делает этот молекулярный механизм видимым. В этом процессе используются радиоактивные трейсеры, такие как галлий-68 или фтор-18, которые позволяют мне просканировать всё тело с головы до пят и детально отобразить эту молекулу.
В клетках рака предстательной железы ПСМА сверхэкспрессирован — то есть на поверхности клеток наблюдается особенно высокая плотность этого фермента. Эта плотность также служит маркером или индикатором того, насколько агрессивна опухоль. Мы знаем, что опухоли, которые очень сильно сверхэкспрессируют ПСМА — даже и в самой предстательной железе без каких-либо метастазов — уже имеют серьёзное прогностическое значение для того, как заболевание будет развиваться.
А теперь, если наблюдается достаточно высокая сверхэкспрессия ПСМА, я знаю, что могу прицельно воздействовать на него терапевтически. Чем выше экспрессия ПСМА — и множество исследований это подтвердили — тем выше терапевтическая доза, которую можно доставить непосредственно в раковые клетки, потому что ПСМА поглощается этими клетками. Это позволяет мне облучать раковые клетки изнутри и, в зависимости от используемого радионуклида, также воздействовать на соседние клетки.
Вот почему ПСМА-ПЭТ/КТ настолько важна — во-первых, как входной этап для терапии, а во-вторых, чтобы проверить, есть ли где-то в организме у пациента метастазы, которые тоже сверхэкспрессируют ПСМА, а не должны там находиться. И, конечно, я могу использовать эту визуализацию и позже, после лечения — будь то радиолигандная терапия, антигормональная терапия, химиотерапия или лучевая терапия — в качестве контрольного метода, чтобы увидеть, насколько эффективно были „обработаны“ раковые клетки.
PM: Что происходит во время терапии радиолигандами ПСМА?
MХ: Радиолигандная ПСМА терапия использует то обстоятельство, что — как я уже доказал с помощью ПЭТ-сканирования (или, к сожалению, в некоторых случаях не доказал, поскольку могут существовать и ПСМА-негативные или слабоэкспрессирующие метастазы) — эта целевая структура, по крайней мере предположительно, присутствует в организме.
Теперь я делаю следующее: заменяю радионуклид, использованный в ПЭТ-сканировании — галлий-68, фтор-18 или иногда медь — на терапевтический радионуклид. Это означает, что я использую тип излучателя, который выделяет так называемое корпускулярное излучение или излучение частицами. В большинстве случаев, когда я использую лютеций-177, это так называемый бета-излучатель, то есть он испускает электроны. Но я мог бы использовать и другие радионуклиды — возможно, мы ещё вернёмся к этой теме.
Радиофармпрепарат, как мы его называем, затем связывается с раковой клеткой и поглощается ею — в данном случае через ПСМА. Но на этот раз цель не в том, чтобы её визуализировать, а в том, чтобы оказать терапевтический эффект.
И вот что происходит — то, что радиация, будь то внешняя или внутренняя, по сути делает с клеткой: в идеале она начинает разрушать ДНК раковой клетки. Цель — повредить её настолько сильно, чтобы клетка больше не могла делиться, позволяя организму постепенно разрушить и устранить опухоль.
PM: Вы используете разные радионуклиды — когда и какой из них Вы выбираете?
MХ: Да — на самом деле мы предлагаем несколько разных радионуклидов. С одной стороны, это лютеций, бета-излучатель, который уже широко используется — его уже более десяти лет применяют при РПЖ и ещё дольше при других опухолях, поскольку у него отличные свойства: само бета-излучение, его период полураспада и глубина проникновения в ткани, которая составляет примерно от одного до двух миллиметров.
Но мы также обнаружили — а это сейчас очень быстро развивающаяся область исследований — что другие радионуклиды могут быть чрезвычайно эффективными, иногда даже более эффективными против раковых клеток, и при этом более щадящими для окружающих здоровых тканей.
Одним из важных примеров здесь является актиний — альфа-излучатель, который тоже уже давно применяется, по крайней мере в университетской среде, и сейчас всё активнее проходит клинические испытания. Он особенно хорошо подходит пациентам с обширным поражением костного мозга. Актиний испускает альфа-излучение, которое имеет очень короткую дальность — около одного-двух диаметров клетки в ткани — то есть практически не вызывает побочных эффектов там, где не накапливается.
Единственная проблема, которую мы наблюдали с актинием-ПСМА, — если проводить терапии слишком часто, могут пострадать слюнные железы, которые, к сожалению, тоже экспрессируют этот фермент.
В самом костном мозге, даже у пациентов с тяжёлым его поражением, мы видим очень мало побочных эффектов, возможно, даже меньше, чем с лютецием, потому что дальность излучения настолько мала. Поэтому мы в первую очередь используем актиний в случаях с обширными метастазами в костном мозге.
И вот совсем недавно мы также начали предлагать тербий-161. Здесь всё немного сложнее. Какое излучение испускает тербий? Оно в чём-то сопоставимо с лютецием — тоже имеет бета-компонент, хотя и не такой сильный. Но, помимо этого, он испускает так называемые электроны Оже и конверсионные электроны; я не буду слишком углубляться в детали, потому что это уже технические нюансы, но у этих электронов сверхкороткая дальность.
Это значит, что комплекс, попав внутрь клетки, должен максимально приблизиться к её ядру. Как только это происходит, эти электроны могут высвобождать чрезвычайно высокую энергию и, возможно, обеспечивать ещё более эффективное разрушение клеточного ядра, чем альфа-излучение актиния. И поскольку нам не нужно вводить столько радиоактивности, сколько требуется с лютецием, вероятнее всего, побочных эффектов будет ещё меньше.
Правда, мы пока находимся на начальной стадии — первые проспективные клинические исследования только ведутся. На практике мы применяем тербий, когда пациент уже стал рефрактерным к лютецию и даже к актинию и когда мы хотим попробовать ещё одну возможную терапию — индивидуальную попытку лечения тербием, хотя на данный момент данных по нему пока немного.
PM: Многие клиники предлагают эту терапию в условиях стационара, тогда как Вы лечите пациентов амбулаторно. Почему?
MХ: Рак очень тесно связан с психологией, особенно на разных стадиях болезни — и тем более на ранних стадиях РПЖ, когда всё чаще применяется радиолигандная терапия. Пациенты не хотят, чтобы им напоминали о том, как всё может выглядеть на финальных стадиях. Они также не хотят чувствовать себя запертыми или как будто они серьёзно больны, когда на самом деле сами так себя не ощущают.
Большинство пациентов бодро забегают в клинику и говорят, что вообще не чувствуют своего рака простаты, даже если ПСМА-ПЭТ скан показывает обратное — весь организм в «чёрных пятнах». Именно это и вдохновило нас — мы сами родом из клинической среды, где много лет проводили такую терапию в AKH в Вене (Центральный клинический госпиталь Вены) — посмотреть на ситуацию иначе. До сих пор единственной причиной держать пациентов в стационаре была радиационная безопасность, которая предполагала: «Ну, на всякий случай, давайте оставим пациента минимум на 48 часов», как это до сих пор часто делают в Германии.
Но мы сказали: давайте сядем вместе с органами надзора, проведём тщательные замеры и докажем, что эти пациенты на самом деле не представляют радиационной угрозы для окружающих. Именно это в итоге и позволило нам получить официальное разрешение. И в Австрии тренд — особенно после нашей последней ежегодной конференции — явно движется именно в эту сторону. Все говорят: конечно, амбулаторное лечение с точки зрения радиационной безопасности абсолютно безопасно.
Разумеется, пациентам даются чёткие инструкции, особенно если они собираются находиться в контакте с беременными женщинами или маленькими детьми — в таких случаях им советуют на неделю немного ограничить контакт. Это может означать, например, не навещать внуков или несколько дней не видеться с беременной дочерью. Эти меры предосторожности очень просты и легко выполнимы.
Сама процедура очень короткая — по сути это всего лишь быстрая внутривенная инфузия. И да, пациентам потом нужно пить много жидкости, чтобы помочь вывести вещество через почки, но с этим любой взрослый вполне справится дома. Поэтому на самом деле нет ни малейшей необходимости ради этого держать относительно здоровых пациентов в больничной палате. Конечно, с тяжело больными пациентами ситуация, естественно, совсем другая — с ними всё организуется по-другому.
PM: Чем Ваша терапия отличается от других методов лечения рака?
MХ: Ну, продолжая тему РПЖ, существуют очень чёткие рекомендации, которые при метастатическом процессе уже давно ставят гормональную терапию на первое место. Гормональная терапия в разных формах — будь то блокада выработки гормонов или блокировка андрогенных рецепторов — безусловно, занимает своё место. На практике пациенты часто достаточно быстро видят эффект от гормональной терапии, но, к сожалению, побочные эффекты тоже начинают проявляться довольно быстро.
Конечно, когда речь идёт о раке, всегда остро встаёт вопрос о химиотерапии. И в случае РПЖ — особенно с такими препаратами, как Доцетаксел и Кабазитаксел — результаты, скажем так, довольно скромные. Побочные эффекты при этом весьма значительные, а поскольку рак простаты обычно не является быстрорастущей опухолью, химиотерапии несколько не хватает «мишени».
Наша же цель — это, в конечном счёте, излучение. И хотя мы часто говорим об этом как о лекарственном препарате — а регулирующие органы, такие как EMA и FDA, именно так это и классифицируют — на самом деле, по сути, мы проводим форму радиотерапии. Фармацевтический компонент, лиганд, который присоединяется к раковой клетке, можно ввести в концентрации в десять тысяч раз выше — и он всё равно бы не вызвал никакой реакции в организме. Это было проверено исследованиями. Единственное терапевтическое действие исходит от радиации. А вот какого качества будет это излучение — зависит от того, какой радионуклид мы используем.
По сути, это как дистанционная лучевая терапия — только гораздо более прицельная, потому что воздействует непосредственно на поверхности клетки и при этом по всему организму. Вот это и является принципиальным отличием нашей терапии от внешнего облучения.
PM: Насколько хорошо переносится радиолигандная терапия?
MХ: Мы можем исходить из того, что только что обсудили. Поскольку наша терапия чрезвычайно точна на уровне клеточной поверхности, мы видим относительно мало побочных эффектов. И снова вступает в игру принцип тераностики: сначала я смотрю на ПЭТ/КТ. На ПЭТ/КТ я должен прежде всего увидеть, что метастазы, как минимум, экспрессируют ПСМА более интенсивно, чем другие органы, которые тоже обладают ПСМА.
И поскольку — как я уже говорил — название немного вводит в заблуждение, так как ПСМА на самом деле является фолатгидролазой, ферментом, мы, к сожалению, также находим его и в слюнных железах. Я уже указывал на это. Почки также получают некоторое количество радиации. Другие органы обычно затронуты меньше. Костный мозг тоже получает небольшую дозу, но это обычно обратимо. Проспективные исследования не показали значительных побочных эффектов высокой степени, которые имели бы значимое влияние.
Тем не менее, если проводить много циклов терапии — а мы уже сделали достаточно много повторных процедур — мы можем начать замечать, как функция слюнных желез постепенно снижается со временем. Это и понятно, поскольку они также подвергаются некоторому облучению.
Функция почек обычно подвержена риску только в сочетании с другими препаратами, которые нагружают почки, или если почки уже повреждены, будь то после операции, внешнего облучения, других терапий, химиотерапии и так далее. Поэтому важно постоянно мониторить функцию почек. Правильная гидратация до, во время и после терапии абсолютно необходима. И при хорошей гидратацией, даже при нескольких циклах лечения, мы не наблюдали повреждения почек.
PM: Как Вы проверяете, было ли лечение успешным?
MХ: И здесь снова нам на помощь приходит наша замечательная ПСМА-ПЭТ/КТ. В рамках тераностической концепции я использую ту же цель, как мы её называем, чтобы проверить: исчезла ли она? Конечно, в идеале она больше не должна обнаруживаться. Но нужно помнить, что мы имеем дело с раком, и рак всегда может вернуться. Есть клетки на определённых стадиях клеточного цикла, которые не восприимчивы к повреждениям — как грибковые споры, прячущиеся где-то в ожидании ослабления иммунной системы для активации. Так возникают рецидивы.
Естественно, то, что мы делаем, не является всё излечивающей панацеей — позже могут возникать рецидивы. И если мы что-то обнаруживаем с помощью ПСМА-ПЭТ, но не можем это должным образом разрешить, это иногда связано с разрешающей способностью сканера. Мы не можем визуализировать отдельные клетки — это выходит за рамки возможностей текущей визуализации — но мы можем использовать её как суррогатный маркер. Если ПСМА-ПЭТ больше не обнаруживает никакой активности, и, в идеале, уровень ПСА тоже неопределяем, — предполагая, что у пациента больше нет предстательной железы, потому что в противном случае нормальная ткань простаты всё равно будет производить некоторое количество ПСА, — тогда мы можем говорить о полной ремиссии.
Мы на самом деле можем количественно оценить регрессию метастазов. Мы всегда сравниваем ПСМА-ПЭТ до терапии, измеряя как объём метастазов, так и их экспрессию ПСМА, которая может быть измерена на сканировании. Затем мы сравниваем это с посттерапевтической ПЭТ. Мы уже публиковали исследования, показывающие, что это измерение может служить надёжным суррогатным маркером прогрессирования заболевания у пациента.
PM: Может ли повторять радиолигандую терапию, если рак вернулся?
MХ: Ответ довольно прост — да, в большинстве случаев. Ранее я это упоминал: у некоторых пациентов мы проводили терапию до 18 раз. Мы придерживаемся более строгого протокола, чем тот, что используется с утверждённым препаратом Pluvicto. Мы планируем терапию каждые четыре недели, потому что в университете, когда ещё не было утверждённых препаратов, мы заметили, что более строгий график даёт несколько более высокую процент положительного ответа на терапию, чем в других клиниках. Поэтому мы придерживаемся этого протокола. Раньше мы также использовали немного более высокую дозу. Но после каждых трёх сеансов мы проводили ПЭТ-сканирование, и если видели, что пациент в ремиссии, давали организму немного времени для поддержания ремиссии — что часто приводило к отличным результатам. Если через более длительный период всё ещё что-то обнаруживалось или появился новый метастаз, мы начинали лечение снова. Так что, по сути, мы всегда работали блоками по три сеанса. Мы сохранили этот подход и в нашей частной практике.
На практике, если у пациента нет серьёзных побочных эффектов — особенно касающихся костного мозга или почек — возможно провести до 20 сеансов. Недавняя статья в The Journal of Nuclear Medicine описала случай с 22 сеансами у одного пациента. Так что да — это возможно.
PM: Спасибо, профессор Хартенбах.
MХ: Был очень рад.
FDA одобрила ¹⁷⁷Lu-ПСМА при мКРРПЖ до химиотерапии
FDA одобрила ¹⁷⁷Lu-ПСМА при мКРРПЖ до химиотерапии
Управление по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) расширило показания для ¹⁷⁷Lu-ПСМА-617 (Pluvicto®), одобрив его использование до химиотерапии у пациентов с ПСМА-позитивным метастатическим кастрационно-резистентным раком предстательной железы (мКРРПЖ).
Критерии отбора пациентов:
- ПСМА-ПЭТ-позитивное заболевание
- прогрессирование на фоне андрогендепривационной терапии (АДТ) и одного курса терапии ингибиторами андрогенных рецепторов (ИАР)
Решение принято на основании положительных результатов исследования PSMAfore фазы 3 (NCT04689828).
Сотрудничество с Фондом медстрахования Хорватии (HZZO) по Pluvicto амбулаторно
Сотрудничество с Фондом медстрахования Хорватии (HZZO) по Pluvicto амбулаторно
Мы рады объявить о нашем сотрудничестве с Фондом медстрахования Хорватии (Hrvatski Zavod Za Zdravstvene Osiguranje), который теперь предоставляет своим пациентам доступ к Pluvicto® (ПСМА-радиолигандной терапии) в рамках утвержденных показаний, амбулаторно!
Это гигантский скачок для системы здравоохранения, но всего лишь маленький шаг для пациента, поскольку амбулаторная терапия устраняет необходимость в госпитализации, а сама процедура занимает всего около одного часа.
После недавнего одобрения Pluvicto Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов США (FDA) для применения до химиотерапии, мы надеемся, что Европейское агентство по лекарственным средствам (EMA) и другие государственные медицинские страховые фонды в Европе вскоре последуют этому примеру.
💡 Амбулаторно, комфортно для пациента, эффективно!
Центр передового опыта тераностики Австрии
С гордостью спешим сообщить, что наша клиника получила аккредитацию как Theranostic Center of Excellence (Центр передового опыта в области тераностики) от Европейской ассоциации ядерной медицины (EANM). В настоящее время наше учреждение является единственным в Австрии, удостоенным сертификата EARL.
Отзыв пациента: полная ремиссия после терапии ¹⁷⁷Lu-ПСМА
Отзыв пациента: полная ремиссия после терапии ¹⁷⁷Lu-ПСМА
Вот отзыв одного из наших пациентов:
"Я хотел бы поведать всему миру, что маленькая частная клиника Minute Medical в Вене, возглавляемая профессором Маркусом Хартенбахом, экспертом в области ядерной медицины, является настоящим гигантом в помощи людям, нуждающимся в медицинской помощи, доказав успешное применение новейших научных медицинских исследований в повседневной практике.
Доктор Хартенбах имел смелость пойти против устаревших «универсальных протоколов» в лечении метастатического рака предстательной железы, что является скромной услугой для больных мужчин, которым бы иначе пришлось подвергнуться жестокому и вредному для организма лечению, ухудшающему качество жизни.
О чем идет речь? О терапии, нацеленной на ПСМА, с использованием лигандов Лютеция-177 для лечения метастатического рака предстательной железы, которая обычно трудно или совсем недоступна. По моему опыту, большинство международных врачей следуют «протоколу», согласно которому больные подвергаются общей радиации, химиотерапии и химической кастрации с помощью гормональной терапии, что часто приводит к формированию клеток рака, устойчивых к гормонам, которые больше не поддаются лечению.
Профессор Хартенбах лечит своих пациентов по принципу «индивидуализированного подхода», что означает, что он смело применяет самые современные методы лечения в нужное время. Как это часто бывает в частных клиниках, это пациенты, которые стремятся получить эти терапии за свой счет и на свой страх и риск из желания сохранить свой образ жизни, способность наслаждаться жизнью и свою подвижность, несмотря на ужасную болезнь, которая, по моему мнению, в рамках обычного 'протокола' становится непереносимой для человеческого тела, медленно разрушая все, ради чего стоит жить.
Весь текст пока был составлен преимущественно в третьем лице, чтобы представить мало-мальски объективный отчёт о случае. Однако, к сожалению для меня, я сам страдаю от этого заболевания, и мне потребовался длительный процесс поиска клиники профессора Хартенбаха. Меня зовут Шандор Амбруш, и мне 70 лет.
Я считаю, что мне действительно повезло, что меня проконсультировала мой замечательный семейный врач и терапевт, доктор Андреа Шеленйи из Будапешта, Венгрия, которая обратила моё внимание на существование этой уникальной терапии. Я также благодарен профессору Штефану Фёрстеру из клиники Университета Байройт, который не смог взяться за моё лечение из-за обязательных протоколов в государственных клиниках Германии, но любезно познакомил меня с профессором Хартенбахом.
В январе этого года мне сделали радикальную простатэктомию в Будапеште, и после операции мне диагностицировали метастазы в лимфатических узлах. Я прошел ПСМА-ПЭТ/КТ, которая выявила пораженные узлы. В соответствии с венгерским «протоколом» - идентичным немецкому - мне рекомендовали пройти вышеупомянутые терапии, что вызвало у меня ужас, лишивший меня сна и порождавший кошмары, после которых я просыпался к реальности, ещё более пугающей, чем эти страшные сны. Это продолжалось до тех пор, пока я не встретил профессора Хартенбаха, который убедил меня в моём праве выбора лечения для себя по своему усмотрению.
Я прошел три сеанса терапии лютецием с интервалом в месяц между сеансами. Каждый сеанс продолжался 15 минут, сопровождавшихся приятной образовательной беседой с профессором Хартенбахом о моем здоровье и возможных прогнозах. Я не испытал никаких побочных эффектов ни непосредственно после сеанса, ни до настоящего момента. После завершения лечения я прошел повторную ПСМА-ПЭТ/КТ, которая показала полную ремиссию рака. Конечно, это может измениться со временем, так как с этой болезнью никогда не знаешь, но я надеюсь, что так будет долго. В худшем случае, если болезнь вернется, лечение можно повторить, в зависимости от обстоятельств на тот момент.
Что касается моего текущего состояния, я живу полной жизнью, как и до диагноза. Я также подвижен, как и в последние 50 лет, работаю над своим бизнесом, наслаждаюсь прекрасной семейной жизнью, летаю по Европе хотя бы раз в неделю и несколько раз в год за границу. Я проезжаю на машине десятки тысяч километров в год, и ничего из этого не изменилось с тех пор, как я решил обратиться к профессору Хартенбаху.
С уважением,
Доктор Шандор З. Амбруш"
Эра тераностики — СЕЙЧАС
Эра тераностики — СЕЙЧАС
Европейская ассоциация ядерной медицины (ЕАЯМ) провела свою ежегодную конференцию, EANM24, с 19 по 22 октября 2024 года в Гамбурге, Германия. Конференции EANM известны тем, что демонстрируют последние достижения в области ядерной медицины, которые можно разбить на следующие категории:
- Новые мишени: идентификация новых белков и ферментов в различных видах рака и других заболеваниях
- Новые лиганды: разработка транспортных молекул с улучшенной способностью стыковки
- Новые трейсеры: более мощные радионуклиды с более коротким радиусом радиации, чтобы минимизировать повреждение окружающих здоровых клеток
- Расширенное применение уже известных радиолигандов: открытие известных белков/ферментов в других раках и поражениях.
Как обычно на таких профессиональных встречах, конференция этого года также сосредоточилась на том, как приблизить тераностику к пациентам, освещая технические аспекты, такие как организация клиник, обучение врачей, поток пациентов и улучшение доступа на «последней миле». Стоит особенно отметить одну презентацию из Финляндии, посвященную изучению осуществимости тераностического лечения амбулаторным способом — в чём наша клиника является ярким примером. 1
Упрощение и унификация регулирующих норм на уровне ЕС еще более улучшит доступ пациентов к терапиям в области ядерной медицины, при этом Австрия представляет собой модель для эффективной практики.
ИИ и ядерная медицина
Искусственный интеллект стал важной темой обсуждения, в частности, его потенциал для улучшения ядерной медицины, например, в интерпретации ПЭТ-сканов. Способность ИИ улучшать диагностику может представлять собой значительный прогресс в точности и эффективности.
Применение тераностики на основе ПСМА и ДОТАТАТЕ
Визуализация и терапия на основе ПСМА и ДОТАТАТЕ стали уже стандартом лечения, и более чем десятилетний накопленный клинический опыт теперь идёт на пользу при разработке новых радиофармпрепаратов и мишеней , таких как ФAПи. Одной из основных тем было расширение терапии ПСМА на более ранние стадии рака предстательной железы (РПЖ) и решение проблемы резистентности путём сокращения интервалов лечения — протокол, который наша клиника ввела одной из первых. Наш оптимизированный протокол состоит из трех сеансов с интервалом в четыре недели вместо обычных шести-восьми, опираясь на исследование нашего главного специалиста по ядерной медицине, профессора Хартенбаха. Такой режим снижает адаптивный потенциал рака, оставаясь при этом переносимым для пациентов.
Революционное влияние ПСМА-ПЭТ/КТ на принятие клинических решений подтверждается многочисленными исследованиями, подтверждающими её ценность для улучшения диагностики и выживаемости.2
Новейшие открытия соматостатиновых рецепторов в миеломах и ферментов ПСМА в глиомах открывают перспективы для лечения этих видов рака с использованием целенаправленной радионуклидной терапии.3
Новые мишени
Примерно треть РПЖ не экспрессируют ПСМА, что делает терапию на основе ПСМА неэффективной и требует альтернативных маркеров. Одно исследование выявило высокую экспрессию CD13 при ПСМА-отрицательном РПЖ, что делает белок CD13 потенциальной мишенью для тераностики.4
Разработка новых радиолигандов и радионуклидов
Среди новых радиолигандов – DOTA-LM3, меченый 161Тербием ([161Tb]Tb-DOTA-LM3), который показал семикратное увеличение поглощения опухолью по сравнению с [177Lu]Lu-DOTATOC благодаря улучшенной стыковке двумя связующими точками.5
Тербий-161 также стал перспективной альтернативой дефицитному Лютецию-177. 161Tb обеспечивает более концентрированное излучение с сохранением благоприятного биораспределения. Этот радионуклид излучает β-излучение, аналогичное Лютецию-177, а также терапевтически активные электроны конверсии и электроны Оже, вместе с излучением низкоэнергетического гамма-луча, что позволяет делать снимки с помощью спектральной КТ.6
Белки активации фибробластов (FAPi)
FAPi заслуживает особого внимания. Эти белки, характерные для воспалённых фиброзных тканей, были обнаружены в микроокружении большинства солидных опухолей, предлагая тем самым перспективу для универсальной терапии стромальных раков. Строма играет важную роль в пролиферации рака, питая опухоли и защищая их от иммунного ответа организма. Однако онкологическая реальность гораздо более сложна и неоднородна. Хотя молекулярная визуализация на основе FAPi себя зарекомендовала, терапевтические применения по-прежнему сталкиваются с проблемами, связанными с подходящими лигандами.
Эти основные моменты лишь приоткрывают занавес над знаниями, представленными на EANM24. В будущих публикациях мы углубимся в отдельные темы и исследования, сосредоточив внимание на тех, которые наиболее важны для нашей группы пациентов.
1 OP-093 “Establishing a 177Lu-PSMA treatment site in an oncology outpatient day-ward”, T. Noponen, A. Saikkonen, L. Kääriä, M. Seppänen, K. Mattila, A. Ålgars
2 OP-423 “PSMA-PET and PROMISE re-define stage and risk in prostate cancer patients”, M. Karpinski, J. Hüsing, K. Claassen, L. Möller, H. Kajüter, F. Oesterling, V. Grünwald, L. Umutlu, H. Lanzafame, T. Telli, A. Merkel-Jens, A. Hüsing, C. Kesch, K. Herrmann, A. Stang, B. Hadaschik, W. P. Fendle
3 OP-359 “Assessing the theranostic potential of SSTR imaging in advanced multiple myeloma patients - the SCARLET trial”, W. Delbart, I. Karfis, M. Vercruyssen, S. Vercauteren, Z. Wimana, N. Meuleman, P. Flamen, E. Woff
OP-514 “First-In-Human Experience of Peptide Receptor Radionuclide Therapy with 177Lu-DOTATATE in Patients with Advanced Multiple Myeloma”, W. Delbart, I. Karfis, M. Vercruyssen, S. Vercauteren, Z. Wimana, N. Meuleman, P. Flamen, E. Woff
EP-0113 “Diagnostic utility of 68Ga-Prostate-Specific Membrane Antigen-11 PET/CT in glioma recurrence - a prospective analysis”, A. Meena, K. Subramanian, R. Kumar, H. Singh, B. Mittal
EP-0653 “68Ga/177Lu-PSMA theranostics in recurrent high-grade glioma - First study results & future perspectives”, A. Karlberg, B. E. Vindstad, E. M. Berntsen, H. Johansen, T.M. Keil, O. Solheim, S. Kjærnes Øen, T. Skeidsvoll Solheim, L.Eikenes
4 OP-424 “CD13 as a Potential Membrane Marker in PSMA-Negative Prostate Cancer: A Complementary or Superior Alternative to PSMA”, Y. Tang, L. Xiao, J. Yang, J. Hou, J. Hong, A. Rominger, K. Shi, S. Hu
5 OP-252 “Therapy with the somatostatin receptor antagonist DOTA-LM3 labeled with terbium-161: Interim results of the Phase 0 Study in patients with gastroenteropancreatic neuroendocrine tumors”, J. Fricke, F. Westerbergh, L. McDougall, C. Favaretto, E. Christ, G. Nicolas, S. Geistlich, F. Borgna, M. Fani, P. Bernhardt, N. van der Meulen, C. Müller, R. Schibli, D. Wild
6 OP-515 “When Lutetium-177 DOTATATE Is Not Available: Insights Into Use of Terbium-161 in the Treatment of Metastatic Paraganglioma”, N. Jacobs, O. Kolade, K. Hlongwa, S. More
OP-529 “Mixed-LET 161Tb-ART-101 radiopharmaceutical enhances therapeutic responses in advanced prostate cancer”, M. Bio Idrissou, J. Tromp, H. Comas Rojas, L. Lambert, A.
Pinchuk, Y. Medina, A. Carston, R. Hernandez
OP-532 “Development of [161Tb]Tb-DOTA-HYNIC-panPSMA for targeted radionuclide therapy of prostate cancer”, C. Morgat, D. Vimont, K. Attia
Результаты испытания UpFrontPSMA: Терапия ПСМА выходит на первый план лечения рака предстательной железы
Результаты испытания UpFrontPSMA: Терапия ПСМА выходит на первый план лечения рака предстательной железы
На конференции ESMO 2024 в Барселоне объявлены результаты клинического испытания UpFrontPSMA, и они действительно обнадёживают, что касается будущего лечения РПЖ. Радиолигандная терапия 177Lu-ПСМА (РЛТ) сделала значительный шаг вперёд в протоколе лечения, теперь опережая химиотерапию доцетакселом. Первоначально введённая после испытания VISION как терапия последней линии для запущенного метастатического кастрационно-резистентного РПЖ у пациентов, подвергшихся интенсивному предварительному лечению, эта РЛТ показала замечательную эффективность и благоприятный профиль безопасности, что позволило ей выдвинуться, так сказать, на передовую лечения. На самом деле, даже кажется, что чем раньше она применяется, тем более она эффективнa.
Обзор испытания
Фаза 2 испытания UpFrontPSMA оценивала эффективность применения 177Lu-ПСМА до доцетаксела по сравнению с только доцетакселом у пациентов, у которых был только что диагностирован метастатический гормоночувствительный РПЖ (мГЧРПЖ) большого объёма. Экспериментальная группа получила два цикла 177Lu-ПСМА (по 7,5 ГБк каждый), за которыми последовало шесть циклов доцетаксела, в то время как контрольная группа получила только доцетаксел. Основной конечный результат заключался в достижении недетектируемого уровня простат-специфического антигена (ПСА) после 48 недель — довольно высокая планка для успеха.
Критерии отбора участников
Ключевым критерием отбора была высокая экспрессия ПСМА, при этом пациентам требовалось продемонстрировать SUVmax выше 20 на основе сканирования 68Ga-ПСМА ПЭТ/КТ. (Как сообщили исследователи, некоторых пациентов пришлось исключить, несмотря на первоначальное наличие ПСМА-активных очагов. Это исключение произошло из-за того, что андрогенная депривационная терапия (АДТ) до начала лечения привела к снижению экспрессии ПСМА.)
Побочные эффекты
Комбинация 177Lu-ПСМА с доцетакселом не привела к увеличению токсичности. Наиболее распространённые серьёзные побочные эффекты были одинаковыми в обеих группах:
- фебрильная нейтропения (11% в экспериментальной группе с комбинацией против 10% в контрольной группе с доцетакселом) и
- диарея (6% в группе с комбинацией против отсутствия в контрольной группе).
Единственный отличный побочный эффект в экспериментальной группе — это сухость во рту, известный побочный эффект 177Lu-ПСМА. Но даже этот был только 1 степени, то есть очень лёгкий.
Будучи целевой терапией, 177Lu-ПСМА хорошо переносится с меньшим количеством побочных эффектов, что приводит к улучшению качества жизни. В отличие от доцетаксела, который вызывает быстрое снижение качества, пациенты, получавшие 177Lu-ПСМА, дольше сохраняли хорошее самочувствие, при этом качество жизни снижалось только после введения доцетаксела.
Анализ протокола
Возникли некоторые опасения, что экспериментальную группу, возможно, недодозировали, поскольку применили только два цикла 177Lu-ПСМА. Обычно применяют три цикла. Однако дизайн испытания был направлен на то, чтобы избежать задержек в стандартном лечении доцетакселом.
В качестве примечания, наша клиника придерживается более строгого протокола с интервалом в четыре недели между циклами, а не шесть-восемь, основываясь на исследованиях профессора доктора Хартенбаха, нашего ведущего специалиста. В целом, немецкие университетские клиники, сыгравшие ключевую роль в разработке ПСМА-таргетных терапий в начале 2000-х годов, накопили значительный опыт в этой области.
Результаты
Результаты испытания были весьма обнадёживающими. У 41% пациентов в группе 177Lu-ПСМА плюс доцетаксел по окончании 48 недель ПСА в крови не выявился, по сравнению с только 16% в группе с доцетакселом. Эта значительная разница демонстрирует превосходящую противоопухолевую активность терапии 177Lu-ПСМА перед доцетакселом, без увеличения токсичности. Эти результаты обещают привести к изменениям в стандартах лечения и ввести 177Lu-ПСМА в лечение мГЧРПЖ на самом раннем этапе.
Клиническое исследование WARMTH: радиолигандная терапия ²²⁵Ac-ПСМА в лечении метастатического рака предстательной железы
Клиническое исследование WARMTH: радиолигандная терапия ²²⁵Ac-ПСМА в лечении метастатического рака предстательной железы
Это многоцентровое ретроспективное клиническое исследование, инициированное WARMTH[*], изучило эффективность и безопасность радиолигандной терапии (РЛТ) ²²⁵Ac-ПСМА в лечении метастатического кастрационно-резистентного рака предстательной железы (мКРРПЖ). В исследовании приняли участие бы 488 мужчин из Австралии, Индии, Германии и Южной Африки в возрасте от 37 до 90 лет. Большинство пациентов ранее прошли несколько курсов иных терапий, включая химиотерапию, ингибиторы рецепторов андрогенов или РЛТ ¹⁷⁷Lu-ПСМА.
Результаты показывают, что у 73% пациентов наблюдалось снижение уровня ПСА после хотя бы одного цикла РЛТ ²²⁵Ac-ПСМА, при этом у 57% снижение составило 50% или более. Несмотря на такие распространённые побочные эффекты, как ксеростомия и токсичность для костного мозга (со значительной превалентностью нарушений работы костного мозга, наблюдаемых до начала лечения), терапия в целом хорошо переносилась, даже у пациентов с уже имеющимися нарушениями.
Так как исследование носило ретроспективный характер, РЛТ ²²⁵Ac-ПСМА часто применялась в качестве терапии последней линии, когда все другие варианты были исчерпаны и оказались неэффективными.
Было выявлено статистически значимое соответствие между снижением уровня ПСА на 50% и более, отсутствием определённых видов предыдущего лечения, отсутствием отдельных метастазов и отсутствием анемии при начале терапии ²²⁵Ac-ПСМА с продлением как безрецидивной, так и общей выживаемости. Однако количество курсов лечения не коррелировало с улучшением безрецидивной или общей выживаемости.
В заключение, РЛТ ²²⁵Ac-ПСМА показала значительный противоопухолевый эффект при мКРПЖ, даже у пациентов с нарушениями функции костного мозга и почек. Влияние предыдущих терапий и метастатической нагрузки на время до смерти или прогрессирования заболевания предполагает, что пациенты с относительно меньшей степенью запущенности могут извлечь большую пользу из терапии ²²⁵Ac-ПСМА.
Наша клиника предлагает своим пациентам с соответствующим профилем заболевания комбинированную терапию 1 + 2 (один сеанс ²²⁵Ac-ПСМА + два сеанса ¹⁷⁷Lu-ПСМА).
[*] WARMTH – World Association of Radiopharmaceutical & Molecular THerapy
| Возраст, лет | |
| Средний | 68·1 (8·8) |
| Диапазон | 37–90 |
| Страны | |
| Австралия | 57 |
| Индия | 111 |
| Германия | 72 |
| Южная Африка | 248 |
| ПСА перед началом, ng/mL | |
| Медиана (IQR) | 169·5 (34·6–519·8) |
| Предыдущие терапии мКРРПЖ | |
| Доцетаксел | 324 (66%) |
| Кабазитаксел | 103 (21%) |
| Абиратерон | 191 (39%) |
| Энзалутамид | 188 (39%) |
| РЛТ ¹⁷⁷Lu-ПСМА | 154 (32%) |
| Радиум-223 дихлорид | 18 (4%) |
| Картина болезни | |
| Костные метастазы | 435 (89%) |
| Лимфоузловые метастазы | 352 (72%) |
| Висцеральные метастазы | 99 (20%) |
| Перитонеальные метастазы | 8 (2%) |
Преобразование рака из смертельного заболевания в хроническое. Результаты после 2 курсов терапии ¹⁷⁷Lu-ПСМА
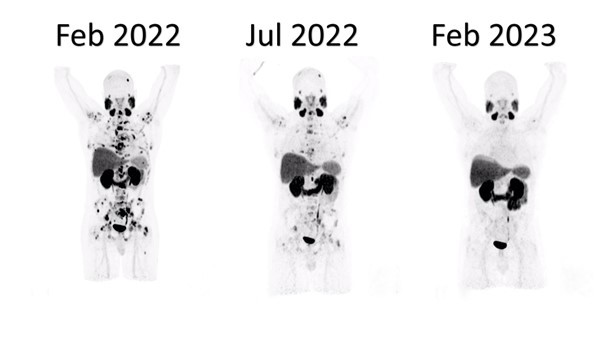
Преобразование рака из смертельного заболевания в хроническое. Результаты после 2 курсов терапии ¹⁷⁷Lu-ПСМА
Этот случай служит иллюстрацией к научным выводам о том, что радиолигандная терапия 177Lu-ПСМА безопасна и эффективна и может успешно применяться несколько раз в случае рецидива, приближая нас к цели превращения рака из смертельного в хроническое заболевание, как и любое другое. Эта терапия также обеспечивает пациентам значительно лучшее качество жизни, чем затяжная андроген-депривационная терапия (АДТ) или химиотерапия.
У 72-летнего пациента Уильяма Дейли впервые был диагностирован рак предстательной железы (РПЖ) в декабре 2021 года. Несмотря на интенсивное предварительное лечение с несколькими циклами иммунотерапии, криоабляции и лейкинтерапии, заболевание продолжало прогрессировать, распространяясь на лимфатические узлы. Пациент отказался от постоянной антигормональной терапии и химиотерапии из-за побочных эффектов и остановил свой выбор на таргетной радиолигандной терапии 177Lu-ПСМА. Пациент прошел 2 курса по 3 сеанса терапии в каждом. После первого курса РПЖ ушёл в ремиссию на 1,5 года.
| ДО 1-го курса | ПОСЛЕ 1-го курса |
| ПСМА ПЭТ/КТ октябрь 2021 г.
ПСА 45 нг/мл Метастазы в лимфатические узлы с высокой экспрессией ПСМА. |
ПСМА ПЭТ/КТ апрель 2022 г.
ПСА 0,18 нг/мл. После 3-x сеансов 177Lu- ПСМА терапии с декабря 2021 г. по февраль 2022 г. наблюдалась значительная ремиссия метастазов в забрюшинных и локорегионарных лимфатических узлах. Снижение ПСА было зафиксировано до октября 2022 года с надиром на уровне 2,39 нг/мл. |
| ДО 2-го курса | ПОСЛЕ 2-го курса |
| ПСМА ПЭТ/КТ сентябрь 2023г.
ПСА 23,3 нг/мл Прогрессирующее заболевание забрюшинных лимфатических узлов с двумя новыми поражениями костей, а также прогрессирование в простате. Повтор 3-х сеансового курса радиолигандной терапии 177Lu-ПСМА через 1,5 года после первого. Для увеличения экспрессии ПСМА была параллельно проведена краткая комплементарная АДТ с Релуголиксом. |
ПСМА ПЭТ/КТ апрель 2024г.
ПСА 0,1 нг/мл После 3-х сеансов радиолигандной терапии 177Lu-ПСМА с декабря 2023 г. по февраль 2024 г. активность в метастазах не выявлена. Единственным зафиксированным побочным эффектом была кратковременная легкая тошнота и легкая усталость после сеанса. Тем временем пациент прекратил приём всех лекарств и сообщает о хорошем самочувствии и восстановлении сил. |
Прочитайте историю г-на Дейли из уст самого пациента :
"Моя история началась в декабре 2014 года, когда мне поставили диагноз РПЖ. Рак был оценен как «среднего риска» с баллом 7 (3+4) по шкале Глисона в 3 из 12 взятых образцов биопсии. На этом этапе рак не метастазировал, но после МРТ было выявлено «внекапсулярное распространение». Я решил не делать операцию и выбрал выжидательную тактику. Я также хотел избежать гормональной терапии.
После ещё одной МРТ выяснилось, что РПЖ находится очень близко к семенным пузырькам, и я обратился к врачу в Форт-Лодердейле, штат Флорида, чтобы он помог мне с лечением. Он провёл 3D-биопсию, которая показала Глисон 8 в предстательной железе. Затем он провёл фокальную криоабляцию, и мой ПСА снизился с 9 до 0,6. Это было сделано в октябре 2017 года.
ПСА продержался на этом уровне около 2 лет, прежде чем начал постепенно расти. Так получилось, что в июле 2020 года мне лечили камень в почке, и в области таза был замечен увеличенный лимфатический узел. После еще одной МРТ мой врач во Флориде предложил пройти иммунотерапию. Его иммунотерапия хорошо показала себя у некоторых пациентов, но в моём случае она оказалась безрезультатной. Тогда мы начали рассматривать вариант терапии 177Lu-ПСМА у доктора Хартенбаха. Сначала мне сделали сканирование ПСМА в Хьюстоне, штат Техас, чтобы выяснить, подойдёт ли мне терапия. После одобрения я организовал лечение у доктора Хартенбаха. В то время мой ПСА составлял около 48. Это было осенью 2021 года.
После 1 курса (3 инфузий) терапии мой ПСА составил 2,39. Контрольное сканирование ПСМА показало значительное улучшение. Остались всего лишь несколько мест, где рак всё ещё находился в процессе отмирания. Мы остались очень довольны результатами лечения. Это было весной 2022 года, и терапия подарила мне 2 года ремиссии. После тщательного наблюдения за раком со всеми запланированными анализами ПСА снова начал расти. Когда он достиг 23, мы решили, что дополнительная терапия имеет смысл.
Поэтому в декабре 2023 года я начал еще один цикл терапии 177Lu-ПСМА. Мы также сопроводили терапию препаратом Орговикс. Сканирование ПСМА было проведено в апреле после завершения лечения в феврале 2024 года. Думаю, я могу сказать, что испытал минимальные побочные эффекты от лечения (легкая тошнота в течение нескольких дней и небольшая сухость во рту). Таким образом, меня пролечили 2 курсами (всего 6 инфузий) у доктора Хартенбаха.
На этот раз результаты лечения и сканирования оказались замечательными. Скан ПСМА был чистым, и в заключении говорилось, что у меня «полная ремиссия» в ответ на терапию — мой ПСА сейчас составляет 0,1. Я не мог бы ожидать лучшего результата, и я очень благодарен и счастлив сотрудничеством с доктором Хартенбахом и его командой. Я молюсь о длительной ремиссии.
Ещё раз благодарю доктора Хартенбаха и всю его команду."
Прорыв в лечении рака молочной железы: первый тераностический метод с использованием DOTATATE. Настал поворотный момент?

Прорыв в лечении рака молочной железы: первый тераностический метод с использованием DOTATATE. Настал поворотный момент?
Недавнее исследование выявило гиперэкспрессию соматостатиновых рецепторов типа 2 (SSTR2) в опухолях некоторого типа рака молочной железы, в частности гормонозависимых ER+. Это открытие открывает путь к потенциальному использованию хорошо известной тераностической терапии DOTATATE в целях улучшения диагностики и лечения этого типа рака молочной железы. Исследование, включающее доклинические и клинические испытания второй фазы, продемонстрировало многообещающие результаты.
«Эта терапия вернула меня к жизни.»
"Эта терапия вернула меня к жизни."
История успеха после 3-x сеансов радиолигандной терапии ПСМА с 1x актинием-225 и 2x лютецием-177
У Шона Кенни впервые диагностировали рак простаты в декабре 2020 года, когда ему только исполнился 51 год. Прежде чем попасть в нашу клинику, он прошёл несколько курсов лечения, включая 6-кратный курс доцетаксела, антигормональную терапию, иммунотерапию и криотерапию. Он решил приостановить АДТ из-за побочных эффектов, но в середине 2023 года ему пришлось возобновить антигормональную терапию фирмагоном и апалутамидом. Рак всё ещё прогрессировал со всё возрастающим поражением костей. Несмотря на положительную реакцию на уровне ПСА, боль и экспрессия ПСМА сохранялись. Ему прописали морфин для облегчения боли. Левый тазобедренный сустав был настолько сильно повреждён, что его пришлось заменить. После 3 лет лечений Шон выбрал таргетную радиолигандную терапию ПСМА (РЛТ), которая привела к удивительной ремиссии всего за один цикл из 3-х сеансов. В связи с сильным поражением скелета мы рекомендовали провести первый сеанс с актинием-225, а два оставшихся - с лютецием-177. Судите сами.
| ДО
ПСМА ПЭТ/КТ декабрь 2023 г. ПСА 2 нг/мл после реиндукционного лечения антигормональными препаратами и АРПИ. Состояние после замены левого тазобедренного сустава. Сохраняются высокий уровень экспрессии ПСМА в костных метастазах и боль на фоне приёма морфина. |
ПОСЛЕ
ПСМА ПЭТ/КТ Апрель 2024 г. После 1 сеанса радиолигандной терапии 225Ac-ПСМА и 2 сеансов 177Lu-ПСМА с декабря 2023 г. по март 2024 г. ПСА 0,18 нг/мл. Минимальная остаточная активность в ранее обнаруженных очагах скелета, скорее всего, апоптозные тельца. ЩФ снизилось с 570Ед/л до 180Ед/л (норма <150). |
Шон почувствовал облегчение боли через 10 дней после первого сеанса РЛТ ПСМА с актинием-225 и смог отказаться от приёма морфина. Показатели гемоглобина и почек нормализовались после 2-го сеанса РЛТ ПСМА с лютецием-177. Единственным побочным эффектом, который он испытал, была кратковременная лёгкая тошнота и лёгкая усталость после сеанса. На момент контрольной ПСМА-ПЭТ/КТ эти симптомы исчезли. Шон сообщает о хорошем общем самочувствии и восстановлении сил.
Вот история в его собственном изложении:
«Моя история началась ещё в декабре 2020 года, когда мне сообщили, что у меня запущенный рак простаты, который распространился на лимфатическую систему. Это было обнаружено с помощью обычного анализа крови, когда мне исполнилось 50 лет и в анализ включили маркер ПСА. В то время у меня не было каких-либо явных симптомов, я всё ещё пробегал милю за 7 минут и вёл очень активный образ жизни.
Мне назначили гормональное лечение в январе 2021 года после того, как я вернулся из больницы Роял Марсден в Великобритании, где мне сделали сканирование ПСМА (я не мог пройти сканирование в Ирландии в течение 9 месяцев). Позже в 2021 году я начал 6-кратный курс химиотерапии (доцетаксел), а затем 4 недели облучения. В начале 2022 года я прекратил гормональное лечение из-за побочных эффектов (ПСА упал до очень низкого показателя). Восстановив силы, я снова вернулся к жизни, и усталость намного уменьшилась.
Затем, в начале 2023 года, ПСА вновь начал медленно повышаться, поэтому мы решили поехать в США, чтобы пройти иммунотерапию и криотерапию в клинике. В ожидании приёма в эту клинику у меня появилась периодическая боль в левой ноге, о которой я сообщил своему онкологу во время амбулаторного визита. После немедленного рентгена ноги мне сказали, что мне грозит перелом бедренной кости и необходима экстренная замена тазобедренного сустава (тазовая кость была также поражена). Через 2 дня мне заменили сустав, и, когда я снова окреп, я поехал в Америку, чтобы пройти процедуру в надежде, что она снова приведёт меня к ремиссии. К сожалению, это лечение не увенчалось успехом, и через месяц после возвращения домой боль в ногах стала невыносимой из-за метастазов в области таза. Мне снова назначили гормональное лечение и сказали, что я снова пройду облучение.
Моя замечательная жена Брид связалась с американской клиникой, чтобы узнать, есть ли другие варианты. Именно тогда меня направили к профессору Хартенбаху, а остальное, как говорится, - достояние истории. Я отказался ото всех обезболивающих и в ближайшем будущем надеюсь отказаться и от обоих гормональных препаратов. Дальше активное наблюдение и, как говорится, держим кулаки, но, безусловно, эта терапия вернула меня к жизни.
Спасибо профессору Хартенбаху и его команде.»
Использование альфа-излучателей в радиофармацевтических препаратах для лечения рака
Использование альфа-излучателей в радиофармацевтических препаратах для лечения рака
В непрекращающейся борьбе с раком радиофармацевтика превратилась в мощное оружие, а альфа-излучатели, такие как актиний-225, астат-211 и свинец-212, быстро завоёвывают популярность. В лечении рака эти альфа-излучающие изотопы произвели революцию, так как таргетная терапия с их применением обладает потенциалом уничтожения злокачественных клеток, при этом сводя к минимуму повреждение окружающих здоровых тканей.
Переосмысление сроков лечения: ¹⁷⁷Lu-ПСМА на ранних стадиях до традиционных методов лечения
Переосмысление сроков лечения: ¹⁷⁷Lu-ПСМА на ранних стадиях до традиционных методов лечения
Радиолигандная терапия (РЛТ) 177Lu-ПСМА с использованием лютеция первоначально получила одобрение в США в качестве крайнего средства после того, как все другие варианты лечения уже исчерпаны. Тем не менее, много исследований в настоящее время изучают потенциал применения этой терапии на более ранних стадиях РПЖ из-за её доказанной безопасности, эффективности и относительно низкого профиля побочных эффектов. На самом деле, радиолигандная терапия очень безопасна. Недавнее исследование показало, что даже 6 сеансов очень хорошо переносятся, что даёт возможность применять эту терапию как поддерживающую в случае рецидива.
¹⁷⁷Lu-DOTATATE в лечении менингиом
¹⁷⁷Lu-DOTATATE в лечении менингиом
Пептид-рецепторная радионуклидная терапия аналогами соматостатина (ПРРТ) за последние две десятилетия значительно продвинулась в лечении нейроэндокринных опухолей (НЭО), пользуясь гиперэкспрессией соматостатиновых рецепторов, характерных для этих опухолей. Те же рецепторы (SSTR1 / SSTR2) присутствуют практически во всех менингиомах, делая ПРРТ подходящим методом лечения. Многие исследования последовательно продемонстрировали эффективность ПРРТ (177Lu-DOTATATE) у пациентов с менингиомами, особенно в продлении выживаемости без прогрессирования (PFS).
Революционное влияние ⁶⁸Ga-ПСМА ПЭТ/КТ на лечение рака предстательной железы

Раскрытие потенциала точности. Революционное влияние ⁶⁸Ga-ПСМА ПЭТ/КТ на лечение рака предстательной железы
В области медицинской диагностики новаторская процедура 68Ga-ПСМА ПЭТ/КТ стала переломным моментом, открыв беспрецедентные возможности для диагностики и лечения РПЖ. Её невиданная доселе точность позволяет врачам визуализировать рак на молекулярном уровне. Она произвела революцию в диагностике, стадировании и индивидуальном подходе к лечению РПЖ, в конечном итоге улучшив результаты для пациентов и изменив весь ландшафт лечения РПЖ. Ниже представлен обзор лишь некоторых из последних исследований.
Ядерная медицина – универсальный инструмент в онкологии
Ядерная медицина может подарить онкологическим больным более длительную и качественную жизнь.
Ядерная медицина является самой быстрорастущей ветвью медицины, особенно в области онкологии. Она чрезвычайно эффективна и имеет мало побочных эффектов, обеспечивая пациентам более длительную и качественную жизнь по сравнению с традиционными методами лечения, такими как химиотерапия. Она также очень универсальна и применяется при лечении многих видов рака. Наша клиника предлагает не только самые передовые методы лечения, такие как радиолигандная терапия ПСМА с 177Lu и 225Ac, а также 177Lu-Dotatate, но и новейшую диагностическую процедуру 68Ga-FAPI ПЭТ/КТ. Эта процедура особенно хорошо подходит для таких видов рака, как рак молочной железы, толстой кишки и поджелудочной железы, и представляет собой новаторский подход к точной диагностике. Здесь вы можете узнать больше о FAPI в диагностике.
¹⁷⁷Lu-ПСМА терапия безопасна и эффективна для пациентов старше 80
¹⁷⁷Lu-ПСМА терапия безопасна и эффективна для пациентов старше 80
Клиническое исследование, оценивающее эффективность и безопасность радиолигандной терапии 177Lu-ПСМА для лечения мКРРПЖ у пациентов восьмидесяти лет и старше, показало, что эта терапия безопасна и эффективна также для пожилых. Более того, пациенты, которые ранее не проходили химиотерапию, продемонстрировали лучший и более длительный ответ на лечение как с точки зрения общей выживаемости, так и выживаемости без прогрессирования.
Комбинация стереотаксической лучевой и ¹⁷⁷Lu-ПСМА терапий
Комбинация стереотаксической лучевой и ¹⁷⁷Lu-ПСМА терапий
Основная сложность лучевой терапии в лечении рака заключается в достижении оптимального уровня радиации в опухолях и метастазах, который бы эффективно уничтожал раковые клетки, при этом сводя вред для окружающих здоровых тканей к минимуму. Комбинация стереотаксической лучевой терапии (SBRT) и внутренней радиолигандной терапии (РЛТ) 177Lu-ПСМА, по-видимому, является способом максимизировать лечение олигометастатического рака предстательной железы.
Недавнее исследование продемонстрировало значительное увеличение медианы биологически эффективной дозы (BED) до 159 Гр совместным применением 177Lu-ПСМА РЛТ и SBRT. Важно отметить, что это было достигнуто без существенных побочных эффектов, в то время как лишь внешнее облучение обычно не превышает 70 Гр. SBRT, стратегически применяемая после РЛТ, точно нацеливается на любые оставшиеся ПСМА-положительные метастазы, для локализации которых после РЛТ проводится контрольная ПСМА ПЭТ/КТ.
В сотрудничестве с нашими партнерами, специализирующимися на таких видах лечения как кибер-нож, SBRT и протонная/С-ионной терапии, наша клиника координированно предлагает все эти методы лечения. Мы стремимся предоставить нашим пациентам передовое онкологическое лечение, обеспечивая точность и высочайшие стандарты ухода.
⁶⁸Ga-FAPI ПЭТ/КТ превосходит ¹⁸F-ФДГ в диагностике рака поджелудочной железы
68Ga-FAPI ПЭТ/КТ превосходит 18F-ФДГ в диагностике рака поджелудочной железы
Рак - коварное заболевание. Он формирует специфическую микросреду еще до появления самих раковых клеток, что затрудняет его диагностику на решающей ранней стадии. Благодаря новому «трейсеру» для обнаружения альфа-рецептора FAP на фибробластах, связанных с раком (CAF), теперь можно выявить эти «отпечатки пальцев» рака, подобно дактилоскопическому порошку. Раннее диагностирование кардинально улучшает принятие терапевтических решений, что и продемонстрировало новейшее исследование.
Другое исследование подтвердило превосходство 68Ga-FAPI ПЭТ/КТ над 18F-ФДГ, столпом онкологической диагностики, в выявлении метастазов и рецидивов локальных злокачественных новообразований у пациентов с запущенным метастатическим раком поджелудочной железы. Более того, интенсивность (SUV) очагов на снимках была выше. FAPI нацелен на микросреду солидных опухолей, которая особенно характерна для таких видов рака, как саркома, рак молочной железы, толстой кишки и поджелудочной железы. Излишне говорить, что более точная диагностика обеспечивает лучший выбор терапии. 68Ga-FAPI предлагается в нашей клинике. Свяжитесь с нами для консультации и записи.
Подробнее о диагностике FAPI читайте здесь.
Тербий-161 в радиолигандной терапии
Тербий-161 в радиолигандной терапии
Радиолигандная ПСМА-терапия изотопом лютеция 177Lu доказала свою высокую эффективность против метастатического рака предстательной железы. Тем не менее, всё ещё остаётся доля пациентов, на которых это лечение не оказывает своего действия. Возможной причиной может являться недостаточная доза облучения раковых клеток, так что им удаётся выжить. Поэтому сейчас ученые экспериментируют с другим изотопом тербием-161 (161Tb), который наряду с бета-излучением излучает более широкий диапазон энергий, а именно конверсию и Оже-электроны. Тербий-161 обладает свойствами распада, аналогичными 177-лютецию, с периодом полураспада около 7 дней, но более высокой разрушительной силой из-за одновременного излучения электронов конверсии и Оже. Их малый радиус излучения позволяет им высвобождать всю свою энергию непосредственно в раковых клетках, практически не повреждая соседние здоровые клетки.
ПСМА ПЭТ/КТ для оценки эффективности лечения ингибиторами андрогенных рецепторов (ИАР) (энзалутамид)
ПСМА ПЭТ/КТ для оценки эффективности лечения ингибиторами андрогенных рецепторов (ИАР) (энзалутамид)
ПСМА ПЭТ/КТ в настоящее время является столпом онкологического стадирования рака предстательной железы (РПЖ), особенно при наличии метастазов, а также инструментом для подбора подходящего лечения (приемлемость радиолигандной терапии 177Lu-ПСМА). Новейшее исследование установило, что она также может быть использована для оценки эффективности лечения ингибиторами андрогенных рецепторов (ИАР).
Радионуклидная терапия на ранних стадиях заболевания
Радионуклидная терапия на ранних стадиях заболевания
Исследование компании Novartis PSMAfore (клиническое исследование фазы III 177Lu-ПСМА-617 у пациентов с мКРРПЖ, ранее не получавших таксаны) не только достигло своей первичной конечной точки — выживаемости без радиологического прогрессирования (рВБП), но и показало потрясающие результаты, которые могут изменить клиническую практику, как было представлено на конференции ESMO 2023. Радиолигандная терапия (РЛТ) 177Lu-ПСМА-617 у пациентов, не подвергавшихся химиотерапии, привела к медиане рВБП в 12 месяцев по сравнению с 5,6 месяцами в контрольной группе при стандартном лечении. РЛТ также лучше переносится с меньшим количеством побочных эффектов 3-й степени. Результаты могут свидетельствовать о том, что чем в более ранней стадии заболевания применяется РЛТ, тем она эффективнее. Наша собственная клиническая практика, безусловно, это подтверждает.
Эффективность ¹⁷⁷Lu-DOTATATE против гастроэнтеропанкреатических НЭО
Эффективность ¹⁷⁷Lu-DOTATATE против гастроэнтеропанкреатических НЭО
Являясь редким (орфанным) и в общем-то медленно растущим типом рака, некоторые нейроэндокринные опухоли (НЭО) тем не менее ассоциируются с быстрым прогрессированием и плохим прогнозом. Изначальная лицензия 177Lu-DOTATATE (Lutathera®) была выпущена на основании результатов исследования NETTER-1 для неоперабельных НЭО средней кишки. В настоящее время по результатам исследования NETTER-2 177Lu-DOTATATE также продемонстрировала свою эффективность у пациентов с запущенными гастроэнтеропанкреатическими НЭО (ГЭП-НЭО) 2 и 3 степени (G2, G3), причем в качестве терапии выбора или первой линии для впервые диагностированных пациентов.
Спешим поделиться одной из наших историй успеха полной ремиссии
Спешим поделиться одной из наших историй успеха полной ремиссии
| До терапии | После 3-х сеансов радиолигандной терапии ПСМА | Контрольный снимок через год |
Диагностика FAPi ПЭТ
Диагностика FAPi ПЭТ
Белок активации фибробластов (FAP) сверхэкспрессируется в микроокружении опухоли или строме более 90% солидных опухолей, что делает его перспективной мишенью как для терапии, так и для молекулярной диагностики. Молекулярная визуализация, нацеленная на FAP, быстро набирает обороты в диагностике рака. Она особенно подходит в случае раков с сильной десмопластической реакцией (образующей фиброзную ткань), таких как рак молочной железы, толстой кишки и поджелудочной железы.
¹⁷⁷Lu-ПСМА до химиотерапии таксанами
¹⁷⁷Lu-ПСМА до химиотерапии таксанами
После окончания исследования VISION, которое доказало эффективность 177Lu-ПСМА как метода лечения метастазирующего рака предстательной железы, возник следующий вопрос: проявляет ли себя эта терапия ещё более эффективно, если применять её на более ранних стадиях заболевания? Значимое исследование показало, что 177Lu-ПСМА, применяемая до химиотерапии таксанами, действительно более эффективна.
Мета-анализ был разработан для оценки влияния предшествующей химиотерапии таксанами на ответ и выживаемость у пациентов с мКРРПЖ после радиолигандной терапии с 177Lu-ПСМА. Он объединил 13 исследований с участием 2.068 пациентов. Результаты были следующими:
- У пациентов, не получавших таксан, вероятность биохимического ответа была в 1,82 раза выше, т.е. в 1,8 раза выше вероятность отсутствия повышения ПСА.
- Таксан-наивный статус был предиктором как значительно лучшей выживаемости без прогрессирования (более 40%), так и общей выживаемости (более 46%).
В настоящее время проводится еще одно клиническое исследование, посвященное эффективности терапии 177Lu-ПСМА, проводимой параллельно с антигормональной андрогенной депривационной терапией. Результаты ожидаются в III квартале 2024 года.
Персонализированная таргетная радионуклидная терапия — сложна и чувствительна ко времени

Производство радиолигандов
Персонализированная таргетная радионуклидная терапия - сложна и чувствительна ко времени
Производство радиолигандов — это чрезвычайно сложный и чувствительный ко времени процесс, потому что радиофармпрепараты (РФП) должны быть «доставлены» непосредственно в раковые клетки в течение нескольких дней после их синтеза. Это, собственно, то, что представляет собой персонализированная таргетная радионуклидная терапия, поменявшая правила игры в онкологии. Наличие собственной лаборатории и высококвалифицированных радиохимиков помогает нам обслуживать наших пациентов своевременно и с максимально возможной гибкостью.
Гибридная визуализация в диагностике РПЖ
Биомаркеры визуализации ПЭТ-МРТ с двойным трейсером для прогнозирования клинически значимого РПЖ
В некоторых случаях рак предстательной железы (РПЖ) никогда не образовывает метастазы и прогрессирует до клинических симптомов, что определяется как клинически незначимый рак. Точный диагноз, способный дифференцировать клинически значимые и незначимые поражения, приводит к лучшему управлению заболеванием. Последние исследования нашей рабочей группы показали, что комбинированная гибридная визуализация с использованием [18F] фторметилхолина (FMC) ПЭТ и [68Ga]Ga-ПСМАHBED-CC конъюгата 11 (ПСМА)-ПЭТ более чувствительна к выявлению клинически значимого РПЖ по сравнению с только мультипараметрической МРТ. ПСМА ПЭТ является ведущим методом в этом гибридном подходе и на самом деле более надежна, чем только МРТ.
Статистика клиники по радиолигандной терапии ¹⁷⁷Lu-ПСМА
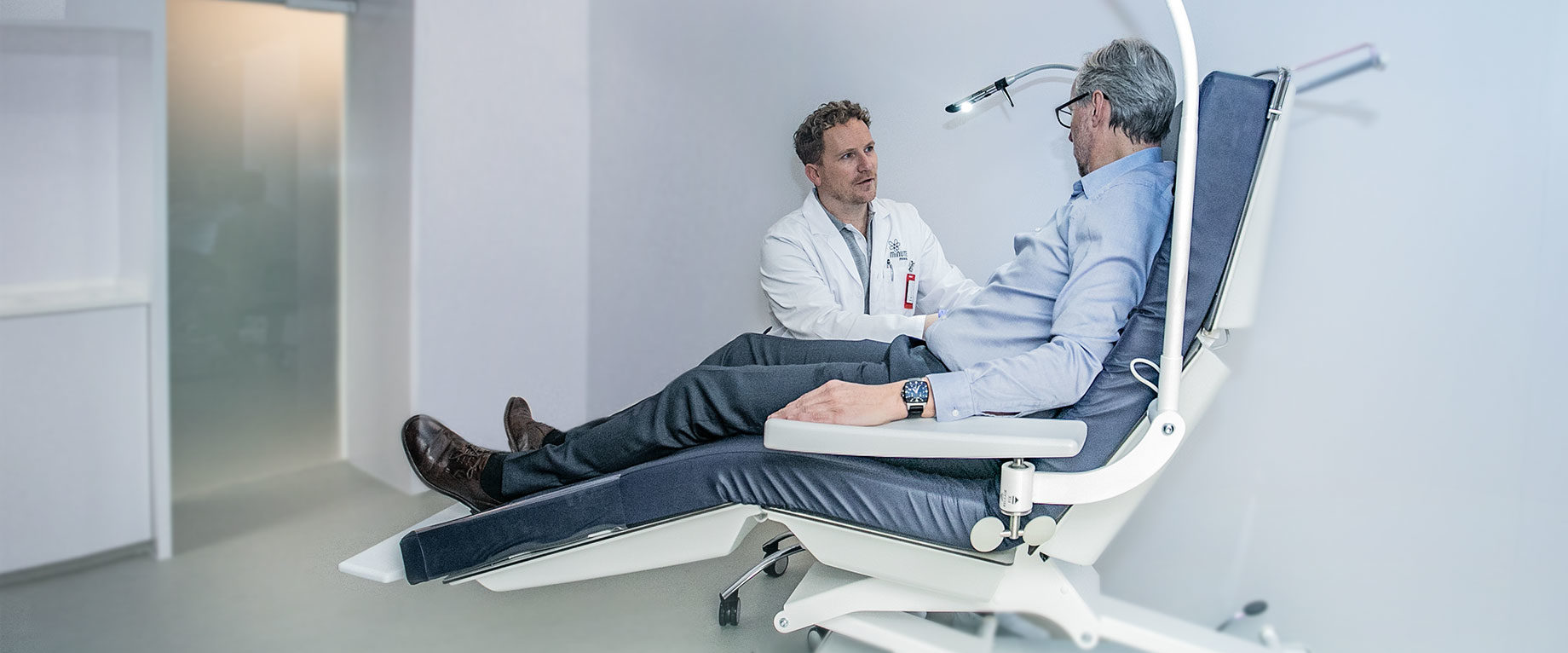
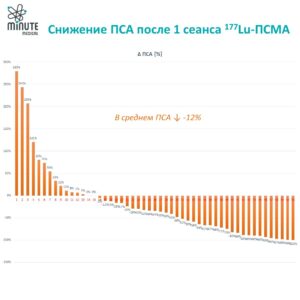
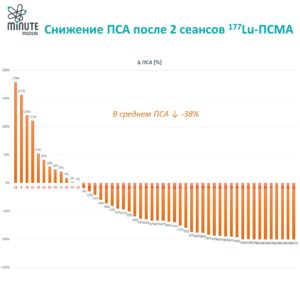
Как показали многочисленные исследования радиолигандной терапии 177Lu-ПСМА, снижение ПСА более чем на 50% приводит к статистически значимому повышению общей выживаемости. Результаты нашей клиники демонстрируют воспроизводимость этих результатов. После 3 сеансов 177Lu-ПСМА ПСА среди наших пациентов снизился в среднем на 68%. Поддержание ремиссии и повышение качества жизни наших пациентов остаются нашими главными целями.
EMA одобрило Pluvicto®
EMA одобрило Pluvicto®
После одобрения американским Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов (FDA) в марте 2022г., в декабре 2022г. Европейское агентство лекарственных средств (EMA) также одобрило Pluvicto® (лютеция-177 випивотид тетраксетан) производства Новартис для таргетной радиолигандной терапии прогрессирующего ПСМА-положительного метастатического кастрационно-резистентного рака предстательной железы. Одобрение EMA основано на результатах исследования ФАЗЫ III VISION, которое продемонстрировало, что «радиолигандная терапия с 177Lu-ПСМА-617 продлевает как выживаемость без радиографической прогрессии, так и общую выживаемость пациентов с прогрессирующим ПСМА-положительным метастатическим кастрационно-резистентным РПЖ при комбинировании со стандартным лечением»[1]. Плувикто® должен применяться одновременно с андроген-депривационной терапией (АДТ) у взрослых пациентов, ранее прошедших лечение ингибиторами андрогеновых рецепторов и химиотерапию таксанами. «Лютеций-177-ПСМА был разработан Немецким онкологическим исследовательским центром (DKFZ) в сотрудничестве с Гейдельбергской университетской больницей и Гейдельбергским университетом».[2]
[1] https://www.nejm.org/doi/full/10.1056/nejmoa2107322
[2] https://www.krebsinformationsdienst.de/aktuelles/2022/news059-metastasierter-prostatakrebs-zulassung-pluvicto-lutetium-177-psma-617-europa.php
Европейская премия в области ядерной медицины 2022 д-р Александр Хауг
Европейская премия в области ядерной медицины 2022
С огромной радостью и гордостью мы сообщаем, что наш коллега профессор д-р Александр Хауг был удостоен Европейской премии в области ядерной медицины 2022.
Интервью с пациентом
Интервью с пациентом, сентябрь 2022г. (на англ.)
Профессор Хартенбах проводит интервью с пациентом о его опыте радиолигандной терапии 177Lu-ПСМА. Пациенту А.Г., самому молекулярному биологу, в сентябре 2018 года в возрасте 69 лет был поставлен диагноз метастатический рак предстательной железы. После обычного стандартного лечения (химио- и антигормональная терапия) все еще наблюдались остатки первичной опухоли в простате, а также метастазы в лимфатических узлах и кости. На сегодняшний день А.Г. прошел 9 сеансов (3 цикла) терапии 177Lu-ПСМА за последние три года, начиная новый цикл каждый раз, когда в результате рутинного контроля 68Ga-ПСМА ПЭТ/КТ обнаруживал раковые очаги, экспрессирующие ПСМА. Терапия показала себя чрезвычайно успешной для А.Г.: высокий ответ и почти никаких побочных эффектов. Таргетная радиолигандная терапия значительно приближает нас к цели сделать рак предстательной железы просто еще одним контролируемым хроническим заболеванием, в то же время сохраняя достойное качество жизни, таким же как, например, диабет.
- [00:45] Можешь ли ты рассказать нам о своём диагнозе рака предстательной железы и первых шагах, которые ты предпринял? Как ты воспринял ограничения, накладываемые стандартными методами лечения, и что побудило тебя искать альтернативы?
- [06:13] Как бы ты оценил побочные эффекты и эффективность радиолигандной терапии по сравнению со стандартными методами лечения?
- [10:07] Каков твой личный опыт с побочными эффектами, такими как сухость во рту (ксеростомия) или проблемы с почками после нескольких циклов радиолигандной терапии?
- [12:00] Важность комбинированного терапевтического подхода, включая гормональную терапию и облучение ионами углерода.
- [15:44] Что лично помогло тебе справиться с болезнью и сохранять оптимизм относительно будущего?
Проф. Маркус Хартенбах (МХ): Здравствуйте и добро пожаловать в Minute Medical. Меня зовут Маркус Хартенбах, и сегодня у нас в гостях особенный человек, который любезно согласился дать интервью — профессор доктор Александр фон Габайн, известный микробиолог, основатель, предприниматель и многое другое. Мы очень ценим, что сегодня он нашел время для этого интервью. Здравствуй, Александр.
А.Г.: Здравствуй, Маркус. Я с нетерпением жду этого интервью и рад поделиться тем, чему научился за время болезни и лечения.
МХ: Да, Александр, мы очень это ценим. Сегодня ты здесь не как аналитический учёный, а потому что четыре года назад — ровно четыре года назад — ты столкнулся с диагнозом. Может, ты немного расскажешь, что это было и какие были первые шаги?
А.Г.: Ну, у меня действительно четыре года назад диагностировали запущенный рак простаты — с метастазами в кости и нескольких лимфатических узлах. И как молекулярный биолог, который сам работал в онкологии, я сразу понял, что это полностью перевернёт мою жизнь. Это шокирующий опыт, и сначала у тебя возникает страх смерти. Поэтому очень важно опереться на коллег, которые зарекомендовали себя и пользуются уважением. Должен сказать, что в университетской клинике мне оказали хорошее лечение. Но была одна дилемма: врачи — возможно, и потому, что я сам из этой сферы — в основном склонялись к стандартным терапиям. Стандартная терапия, конечно, состоит в подавлении тестостерона — что наши коллеги нередко называют кастрацией, будь то химической или физической, — иногда в комбинации с химиотерапией или после неё. Я прошёл через всё это, и были определённые успехи. Но, честно говоря, в моём теле всё ещё были видны остатки первичной опухоли, и сама первичная опухоль оставалась в предстательной железе. Это была серьёзная кривая обучения. И я должен сказать: из этого опыта я вынес, что стандартная терапия важна и полезна. Но когда ты глубоко вздохнёшь и осознаешь: это мой рак и это моя жизнь, надо посмотреть, какие есть ещё возможности. Мне повезло — частично случайно, частично благодаря целенаправленным вопросам среди коллег и друзей, и я узнал, что уже разрабатываются или доступны терапии следующего поколения. И я, конечно, смотрю на всё это глазами молекулярного биолога. Химиотерапия и гормональная ингибиция, которые я прошёл, явно всё ещё медицина ХХ-го века — но не ХХI-го. Почему? Потому что они, конечно, воздействуют на опухоль, но очень далеки от того, чтобы быть действительно специфичными.
Возьмём химиотерапию. Конечно, она блокирует большинство быстрорастущих клеток, и поэтому действует на рак. Но при этом у неё часто бывают очень сильные побочные эффекты на другие ткани организма, которые тоже зависят от делящихся клеток.
Гормональная ингибиция сама по себе — это нормально, но, на мой взгляд, она неспецифична. Она лишает организм тестостерона, который нужен и для других функций, важных для нормального функционирования организма.
Этот опыт стал отправной точкой для поиска других терапий. И что интересно — а это, возможно, преимущество при раке простаты — существует самая специфичная диагностическая методика для обнаружения опухолей или метастазов в организме. Эта методика основана на специфической молекуле, которая связывается с поверхностной структурой клеток рака простаты. Если эту молекулу, например, «пометить» радиоактивным веществом, можно точно определить, где в организме остались опухолевые клетки или метастазы. Когда я проходил эту процедуру несколько раз и видел, что некоторые из предыдущих лечений действительно улучшили моё состояние, я подумал: если этот метод так специфичен в обнаружении отдельных оставшихся раковых клеток — значит, должна быть и терапия, основанная именно на этой специфичности.
И именно так я познакомился с Маркусом — это было не случайно. Я много о нём слышал из разных источников. Маркус объяснил мне, что наука не стоит на месте, и уже усовершенствовали эту ключевую молекулу — которая связывается с рецепторами на поверхности раковых клеток простаты. Присоединив к этой молекуле так называемую «волшебную пулю» (magic bullet), можно направленно применять более сильное излучение. И в сравнении с другими методами лечения, которым я подвергся, это действительно очень-очень специфично. Разрушаются только те клетки, с которыми связывается этот радиолиганд — и он в своём «рюкзаке» несёт радиоизотоп, который целенаправленно уничтожает раковые клетки.
Вот, собственно, история, которую я хотел коротко рассказать — но не будем сейчас слишком углубляться.
МХ: Да, это наша тераностическая концепция, при которой проводится диагностическая процедура с использованием ПСМА-лиганда в ПЭТ/КТ — а затем, конечно, терапия с помощью лигандов ПСМА, меченных лютецием или актинием, которые целенаправленно атакуют раковые клетки. Именно это ты и описал.
Может быть, ты также можешь дать небольшой обзор и сравнить стандартные терапии, которые ты прошёл — и которые действительно привели к успешным результатам, например, в снижении уровня ПСА и уничтожении метастазов в твоём организме — но с точки зрения профиля побочных эффектов. За последние три года ты прошёл девять сеансов терапии ПСМА с лютецием, а последняя процедура была в апреле 2021 года — то есть полтора года назад. Также учитывая возможные долгосрочные побочные эффекты, раз прошло уже полтора года после последнего из девяти сеансов — может быть, ты можешь дать небольшой обзор и сравнить эти формы лечения?
А.Г.: Да, прежде чем перейти к сравнению, хочу ещё раз коротко остановиться на стандартных терапиях, которые я прошёл. Они действительно имели — и я вынужден признать — почти невыносимые побочные эффекты. Честно говоря, во время химиотерапии я временами был настолько истощён, что не мог даже спуститься вниз, не говоря уже о подъёме. Если смотреть с точки зрения молекулярного биолога, это логично: при этом повреждается очень много "невинных" клеток организма, что, как я бы сказал, и приводит к таким тяжёлым физическим нарушениям.
Метод, который только что описал Маркус, отличается своей высокой специфичностью. И я думаю, что самое удивительное в этом: последующее лечение, которое мне тогда предложили коллеги из университетской клиники, состояло из операции и облучения рентгеновскими лучами. Они пытались объяснить, что в моём организме всё ещё остаются несколько очагов раковых клеток, и что с помощью этих двух методов — операции и лучевой терапии — можно улучшить моё состояние. Так что я оказался перед выбором дальнейших неспецифических методов лечения. Ведь ни операция, ни лучевая терапия не могут так точно поразить опухолевые очаги в организме, как описанный метод, который я прошёл девять раз.
И я должен сказать — честно — что у меня практически не было серьёзных побочных эффектов. Я оставался полностью работоспособным. Маркус — не только мой врач, но иногда и мой коуч. Он поощрял меня продолжать вести очень активную профессиональную деятельность. Я не должен был оставить никаких позиций в различных интересных академических институтах или компаниях. Я мог продолжать свою деятельность даже во время лечения. Для меня это было настоящее «алилуя»-ощущение, ведь я занимаюсь молекулярной биологией уже почти 45 или 48 лет. Мои первые учителя были пионерами, которые расшифровали ДНК, открыли первые белковые взаимодействия и объяснили работу клеток. И я подумал: надо же, эти знания действительно дошли до пациентов. Они защищают, потому что уничтожают исключительно — или в основном — раковые клетки или поражённые раком клетки.
Конечно, есть и другие ткани в организме, что представляет собой проблему, это понятно. Но я должен сказать: я не испытал из-за этого никаких ограничений. Если быть честным, единственным заметным побочным эффектом была некоторая усталость. Но я думаю, любое лечение утомляет — даже если просто принимать антибиотики.
МХ: Может быть, мы можем рассмотреть это немного подробнее, потому что многие пациенты боятся известных описанных побочных эффектов радиолигандной терапии — особенно что касается сухости во рту, или ксеростомии. Иногда создаётся впечатление, что в литературе этот эффект несколько преувеличен — именно ксеростомия или сухость во рту. Каков твой опыт после такого большого количества циклов? В литературе обычно описывают до шести циклов. Мы здесь, в Вене, за последние десять лет пролечили множество пациентов, и практически никогда не наблюдали настоящей ксеростомии, то есть настоящей сухости во рту. Аналогично и с почками, хотя комплекс ПСМА экспрессируется в почках, и эти органы тоже упоминаются в литературе. Каков твой личный опыт в этом отношении?
А.Г.: Мой опыт таков, что я до сих пор действительно не страдал от сухости во рту — то есть не было ксеростомии или подобных жалоб в этом отношении. Почки тоже показывают некоторые слабости, но я убеждён, что это связано с другими пройденными мною терапиями — сейчас нет смысла слишком подробно это объяснять.
Но я могу сказать следующее: общее самочувствие во время и после терапии было настолько стабильным, что даже во время лечения можно вести почти нормальную жизнь — не говоря уже о времени после неё. Нет никаких ограничений — ни в личной, ни в профессиональной жизни. И я считаю, что это очень важно, потому что когда у тебя рак, это один из ключевых аспектов качества жизни: продолжать свою обычную жизнь настолько полноценно, насколько возможно.
МХ: В твоём случае также было очень важно — и мы это всегда подчёркиваем — что применялся комбинированный подход. Радиолигандная терапия не является изолированным методом лечения. Ты сначала начал с классического подхода. В течение всего времени мы дополнительно сочетали лечение с антигормональными терапиями — включая препараты третьего поколения. И в качестве последнего этапа лечения была проведена целевая лучевая терапия с использованием ионов углерода, которая также обладает очень высокой точностью. В конце концов, я считаю, именно эта комбинация и стала ключом к успеху.
А.Г.: Да, и в этом контексте я хотел бы вдохновить тех, кто оказался в такой же тяжёлой жизненной ситуации, как и я. Выбирая новые подходы к лечению, человек прежде всего выигрывает одно — время. До того, как я начал радиолигандную терапию — как уже упомянул Маркус — в медицинской практике в основном применялись ингибиторы гормональных рецепторов первого и второго поколения. Некоторые из этих препаратов нужно принимать только вместе с 50 миллиграммами кортизона. Эти терапии действительно имели — и имеют — серьёзные побочные эффекты. Благодаря времени, которое я выиграл с помощью радиолигандной терапии, мне удалось дождаться ингибиторов рецепторов тестостерона третьего поколения. Сейчас я принимаю их параллельно. И здесь снова демонстрируется: молекулярная биология не стоит на месте. Третье поколение — например, Апалутиамид или Даролутиамид — значительно специфичнее первых двух поколений и, соответственно, гораздо лучше переносится с точки зрения побочных эффектов.
Как уже отметил Маркус: у меня в простате остаются — и, надеюсь, лишь они и останутся — некоторые опухолевые клетки. Поэтому мы вместе приняли решение использовать дополнительную технологию, которая прицельно воздействует на предстательную железу, при этом максимально щадя окружающие ткани — прямую кишку и мочевой пузырь. Это была лучевая терапия с использованием ионов углерода. Хотя это и не молекулярно-биологический метод, я бы сказал, что это высокоспецифический физико-химический подход к лечению. На мой взгляд, это настоящий прогресс в лечении данного заболевания, потому что простату можно гораздо точнее облучать по сравнению с классической лучевой терапией с использованием рентгеновских лучей, при которой почти всегда страдает и мочевой пузырь, и нередко — прямая кишка.
МХ: Да, в твоём случае это прекрасно сработало — и, я думаю, для многих других пациентов в том числе. Данные это чётко подтверждают. И, конечно, ты всегда был очень хорошо информирован — в том числе и на научном уровне. Но я хотел бы также поддержать других пациентов: спрашивайте про разные варианты терапии, про методы лечения следующего поколения. Только тот пациент, который хорошо информирован, в конечном итоге получит лучшее лечение.
И последний вопрос — возможно, немного личный и с прицелом на будущее. В чём был твой секрет, твой личный рецепт, чтобы справляться с болезнью — как ранее, так и сейчас? Что помогает тебе сохранять этот позитивный взгляд вперёд?
А.Г.: Ну, я должен сказать: я смотрю в будущее, смотрю вперёд. И я понимаю, что при моей болезни в определённой мере нужна и удача. Но я считаю, что самое главное — что этот процесс обучения, это движение к специфическим взаимодействиям между действующими веществами и целевыми клетками действительно вошло в лечение и значительно его улучшило.
То, что только что упомянул Маркус, мне кажется особенно интересным: есть исследование, которое утверждает — и это захватывающий мысленный эксперимент — что если бы в обществах, которые могут себе это позволить, сегодня же стали применять терапии следующего поколения — не только при раке простаты, но и, например, при диабете или других хронических заболеваниях — то это не только бы значительно сэкономило средства системам здравоохранения, но и существенно продлило бы жизнь пациентов. Этот расчёт действительно проводился. Проблема в том, что терапии следующего поколения часто попадают в практику через «чёрный ход». И «стандарт лечения» иногда становится почти тюремной клеткой для врачей, учёных и, к сожалению, для пациентов.
Я думаю, что то, что я пережил — взяв за ориентир специфичность (я, конечно, привилегирован, ведь я могу понять это с научной точки зрения) — это то, что я всё больше видел: у меня есть хотя бы один путь, который может меня защитить — пока это возможно. И это даёт мне очень много сил.
И я не хочу говорить только о молекулах, науке и терапии — у меня есть семья, которая меня очень поддерживает. Я получил большую поддержку и от доктора Хартенбаха. В этом смысле я вижу его не только как врача, но и как друга и наставника — особенно при важных решениях. Даже в моей личной жизни. Он всегда подталкивал меня продолжать вести как можно более нормальную жизнь.
МХ: Очень красивые слова. Большое спасибо тебе, Александр, за твоё время — и, возможно, в будущем мы продолжим разговор о следующих поколениях терапий. У нас уже есть фибробласт-ориентированная визуализация — и, возможно, на её основе появится и терапия будущего. История продолжается, и жизнь продолжается. Спасибо ещё раз за твои слова и время.
А.Г.: Было очень приятно.
Производство ПСМА-радиолигандов, меченных лютецием-177
Производство ПСМА-радиолигандов, меченных лютецием-177
Таргетная тераностика на основе FAPi для лечения радиойод-рефрактерного дифференцированного рака щитовидной железы
Таргетная тераностика на основе FAPi для лечения радиойод-рефрактерного дифференцированного рака щитовидной железы
Клиническое исследование терапии лютецием-177 на основе FAPi, проведенное Всеиндийским институтом медицинских наук в Нью-Дели, было нацелено на изучение терапевтической эффективности и безопасности 177Lu-DOTAGA.(СА.FAPi)2 у пациентов с радиойод-рефрактерным дифференцированным раком щитовидной железы (РР ДРЩЖ). 15 пациентов с прогрессирующим заболеванием, предварительно уже подвергнутых интенсивному лечению (мин. 2 вида терапии ленватинибом и/или сорафенибом), были отобраны на основе FAPi ПЭТ/КТ. В среднем проводилось по 3 сеанса по 2 ГБк в течение 8-недельного интервала.
TheraP исследование, сравнивающее радиолигандную терапию лютецием с химиотерапией
Клиническое исследование TheraP, сравнивающее радиолигандную терапию лютецием ¹⁷⁷Lu-ПСМА с химиотерапией с использованием кабазитаксела в лечении РПЖ
TheraP, клиническое исследование фазы II, сравнивающее радиолигандную терапию лютецием 177Lu-ПСМА-617 с химиотерапией с использованием кабазитаксела, завершилось явным преимуществом 177Lu-ПСМА перед химиотерапией.
Европейская ассоциация урологов актуализирует свои рекомендации по диагностике и лечению рака предстательной железы
Европейская ассоциация урологов актуализирует свои рекомендации по диагностике и лечению рака предстательной железы
После завершения клинических испытаний Vision, ассоциации урологов постепенно начинают актуализировать свои рекомендации по диагностике и лечению рака предстательной железы (РПЖ). Европейская ассоциация урологов (ЕАУ) теперь настоятельно рекомендует:
- ПСМА ПЭТ/КT (с галлием-68 или фтором-18) как более точный чем КТ и сцинтиграфия костей скелета метод диагностики при стадировании РПЖ высокого риска (ПСА > 20 нг/мл, или Глисон > 7, или клинически пальпируемая опухоль в обеих долях (cT2c)), и
- 177Lu-ПСМА в качестве терапии первого выбора для предварительно пролеченных (АДТ) пациентов с метастатическим кастрационно-резистентным раком предстательной железы (mCRPC) с одним или несколькими метастатическими поражениями, демонстрирующими высокий уровень ПСМА на диагностическом радиомаркированном ПСМА ПЭТ/КТ.
https://uroweb.org/guidelines/prostate-cancer/summary-of-changes
И то, и другое доступно в нашем учреждении. Запишитесь на приём прямо сейчас.
FAPI
Ядерная тераностика: что нас ожидает в будущем?
В то время как тераностика значительно повысила общую выживаемость и качество жизни пациентов с НЭО и раком предстательной железы и становится все более распространенной, наука неустанно работает в направлении следующего важного шага - универсальной панраковой тераностики, базирующейся на белке активации фибробластов (FAP), обнаруженном в опухоль-ассоциированных фибробластах (ОАФ). Для многих широко распространенных видов рака это было бы поистине революционным открытием. Первые исследования ПЭТ/КТ с 68Ga-FAPI, проведенные на людях, продемонстрировали отличные результаты. Дериват лиганда, лучше подходящий для терапевтических целей, находится в пределах досягаемости.
Костные метастазы, рак предстательной железы и тераностика в его лечении
Костные метастазы, рак предстательной железы и тераностика в его лечении
Костные метастазы являются распространенным осложнением многих видов рака, таких как рак молочной железы (70%), предстательной железы (85%), легких и почек (40%), из-за уникальной микросреды костной ткани.
Галлий-68 превосходит фтор-18 в ПСМА-ПЭТ/КТ при стадировании рака предстательной железы
Галлий-68 продемонстрировал превосходство над фтором-18 в цифровой диагностике ПСМА-ПЭТ/КТ для стадирования рака предстательной железы
Фтор-18 является широко используемым изотопом при проведении ПСМА-ПЭТ/КТ для стадирования рака предстательной железы из-за его более длительного периода полураспада и более высокой производственной мощности по сравнению с галлием-68. Последнее исследование, однако, продемонстрировало превосходство галлия-68 из-за очагового неспецифического накопления фтора-18 в костях ребер и таза. Без последующих дополнительных обследований или каких-либо морфологических данных, свидетельствующих о коморбидности, это может быть неправильно истолковано как метастазирование в кости. В то время как неспецифическое накопление в других тканях и физиологическое накопление в ганглиях могут быть отфильтрованы, накопление в костях, как правило, приводит к ложной интерпретации и неправильному диагнозу. Метастазы в кости всё-таки встречаются у 10% пациентов с впервые диагностированным раком предстательной железы и у 80-90% пациентов в запущенной стадии. Чрезмерное стадирование пациента может привести к неадекватным решениям о дальнейшей терапии, особенно в случае раннего биохимического рецидива. Читать далее.
ПСМА терапия с более краткими интервалами в 4 недели
ПСМА терапия по схеме с интервалом всего в 4 недели
Сколько сессий и как часто требует ПСМА терапия с изотопом лютеция? Стандартный цикл состоит из 3 сеансов с интервалом от 6 до 8 недель. Наша более строгая схема из первоначальных 3 сессий с интервалом всего в 4 недели продемонстрировала >80% эффективности даже среди пациентов, прошедших интенсивное предварительное лечение. ПСМА терапии не важно, «где» находятся метастазы: в лимфатических узлах, в костях, в легких, в печени или даже в области самой простаты. Обычные «жертвы» лигандов ПСМА, слюнные железы и почки, не страдают существенно при таком режиме. Подробнее читайте здесь.
Ознакомиться с другими научными публикациями нашей команды по этой теме можно здесь.
ПСМА терапия улучшает качество жизни у пациентов с раком предстательной железы
¹⁷⁷Lu-ПСМА улучшает качество жизни у пациентов с раком предстательной железы
В пятницу, 17 сентября 2021 года, Novartis объявила о новейших положительных результатах исследования VISION: терапия 177Lu-ПСМА-617 тормозит ухудшение физических функций и наступление болевых симптомов у пациентов с метастатическим кастрационно-резистентным раком предстательной железы. Таким образом, наряду с продлением общей выживаемости и безрецидивной выживаемости, эта прорывная терапия также улучшает качество жизни. Читать далее
NCCN добавляет ПСМА-ПЭТ/КТ к рекомендациям по раку предстательной железы
NCCN, ассоциация онкологических центров в США, чьи рекомендации в онкологии применяются для лечения рака, добавила молекулярную визуализацию 68Ga-ПСМА-ПЭТ в свои рекомендации по лечению рака предстательной железы. Кроме того, признавая высокую точность этого вида диагностики в качестве основного и независимого метода, NCCN отказалась от традиционных методов визуализации как необходимого предварительного условия для ПСМА-ПЭТ/КТ. Подробнее читайте в Urology Times.
Объявлены результаты фазы III клинического испытания VISION
23 марта 2021г. компания "Новартис" обнародовала положительные результаты фазы III клинического испытания радиолигандной терапии 177Lu-ПСМА-617 у пациентов с метастатическим кастрационно-резистентным раком предстательной железы (mCRPC) после химиотерапии таксаном и нескольких сеансов андрогенной депривационной терапии (АДТ). Среди пациентов, которые подверглись комбинированному лечению радиолигандами 177Lu-ПСМА-617 и лучшему стандартному лечению, терапия продемонстрировала медиану повышения общей выживаемости в 4,0 месяца, а также медиану выживаемости без прогрессирования рака в 5,3 месяцев в течение медианы наблюдения в 20,9 месяца по сравнению с контрольной группой только с лучшим стандартным лечением.
Преимущества терапии 177Lu-ПСМА-617 продемонстрировали последовательность независимо от применяемого стандартного лечения, демографических характеристик и характеристик заболевания. Снижение простатспецифического антигена (ПСА) на 50-80% (увеличение ПСА обычно ассоциируется с ростом опухоли) также было значительно более распространенно среди группы 177Lu-ПСМА-617.
Эти обнадеживающие результаты привели Новартис к запуску новых исследований в фазе III среди пациентов, которые не подвергались химиотерапии, а также и на еще более ранней стадии - комбинируя 177Lu-ПСМА-617 с антигормональной терапией по сравнению только с антигормональной терапией.
Frontiers in Urology
Frontiers in Urology
Рабочая группа во главе с проф. Хартенбахом продемонстрировала диагностическую ценность ПСМА-ПЭТ/МРТ в случае рака предстательной железы
Рабочая группа во главе с профессором Маркусом Хартенбахом продемонстрировала исключительную диагностическую ценность ПСМА-ПЭТ/МРТ в случае рака предстательной железы, подтвержденного биопсией. ПСМА-ПЭТ/МРТ обеспечило точное стадирование недавно диагностированного рака простаты. Наряду с этим, в результате информации, полученной с помощью гибридной визуализации, стратегия лечения была скорректирована почти для трети пациентов. Научное исследование было опубликовано в журнале Clinical Cancer Research.
Рабочая группа во главе с проф. Хартенбахом продемонстрировала превосходство ПЭТ ПСМА в диагностике рецидива рака предстательной железы
Рабочая группа во главе с профессором Маркусом Хартенбахом смогла продемонстрировать превосходство ПЭТ ПСМА в диагностике биохимического рецидива рака предстательной железы даже при низких уровнях ПСА. Кроме того, этот метод диагностики значительно пополняет информацию, предоставляемую стандартными КТ/МРТ, тем самым приводя к изменениям в стратегии лечения у значительного числа пациентов. ПСМА-положительные поражения были обнаружены у 85,5% пациентов, тогда как у 57,3% МРТ или КТ предварительно не выявили подозрений. Показатели выявления составили 65% при уровне ПСА от 0,2 до <0,5 нг/мл, 85,7% для 0,5-<1, 85,7% при уровне от 1 до <2 и 100% при уровне ≥2. ПЭТ ПСМА привёл к решению об изменениях в лечении у 74,6% пациентов (p < 0,001), причем для 86% из них была назначена терапия, направленная на метастазы. Научная статья была опубликована в журнале «European Journal of Nuclear Medicine and Molecular Imaging».
Маркус Хартенбах получает награду Совета по онкологии «Молодой исследователь»
Маркус Хартенбах получает награду Совета по онкологии «Молодой исследователь» Североамериканской ассоциации ядерной медицины.