Повышение экспрессии ПСМА: как антигормональная терапия помогает радиолигандной терапии
Повышение экспрессии ПСМА: как антигормональная терапия помогает радиолигандной терапии
Радиолигандная терапия (РЛТ), направленная на ПСМА, с использованием таких изотопов, как лютеций-177, актиний-225 или тербий-161, показала впечатляющую эффективность в лечении рака предстательной железы (рпж) при благоприятном профиле безопасности. Такой успех привёл к её более ранней интеграции в схемы лечения.
Тем не менее, у определённой части клеток рака простаты, особенно у пациентов после многочисленных курсов терапии, наблюдается недостаточная экспрессия ПСМА, что делает РЛТ непригодной по текущим критериям визуализации и биомаркеров.
Хорошая новость заключается в том, что низкую экспрессию ПСМА не стоит считать клиническим тупиком. Её можно повысить с помощью фармакологических методов, открывая таким образом возможность применения РЛТ и у этих пациентов. Давайте разберёмся подробнее.
Чем регулируется ПСМА?
В нормальной (доброкачественной) ткани предстательной железы экспрессия ПСМА низкая. Несмотря на вводящее в заблуждение название («простат-специфический мембранный антиген»), ПСМА не является строго специфичным для простаты и вовсе не обилен в клетках предстательной железы. Такое название появилось лишь потому, что ПСМА был впервые обнаружен на поверхности клеток простаты; более точное его название — фолатгидролаза.
Сигнальный путь андрогенного рецептора (AR) — то есть, когда мужские гормоны (андрогены), такие как тестостерон или дигидротестостерон (ДГТ), связываются с андрогенными рецепторами на поверхности клеток, особенно в простате — подавляет экспрессию ПСМА за счёт снижения активности гена FOLH1.
Что работает в одном направлении, действует и в другом: при отсутствии тестостерона (из-за медикаментозного подавления или блокады рецептора) ген FOLH1 — включая его андроген-связывающий участок — активируется, что приводит к (временной) гиперэкспрессии ПСМА. Этот эффект наиболее выражен в клетках с изначально низким уровнем экспрессии ПСМА, как показано в доклинических экспериментах. (Impact of Androgen Receptor Activity on Prostate-Specific Membrane Antigen Expression in Prostate Cancer Cells - PubMed.)
РПЖ, сигнальный путь андрогенного рецептора и ПСМА: сложное взаимодействие
Гормоночувствительный РПЖ зависит от сигнального пути андрогенного рецептора, необходимого для выживания и пролиферации опухоли. Поэтому одним из методов лечения первой линии является блокировка этого пути — либо:
- снижением уровня тестостерона (например, с помощью антагонистов ГнРГ (гонадотропин-рилизинг гормон), таких как Орговикс), либо
- непосредственной блокадой андрогенного рецептора (например, с помощью ингибиторов андрогенных рецепторов, таких как энзалутамид или апалутамид).
На ранних стадиях гормоночувствительного рака ПСМА может временно повышаться в начале андрогенной депривационной терапии (АДТ) (см. механизм выше). Однако спустя несколько недель лечения уровень ПСМА, как правило, снова снижается, так как в отсутствие тестостерона большинство клеток подвергаются апоптозу (запрограммированной клеточной гибели).
К сожалению, часть опухолевых клеток переживает эту депривацию тестостерона и со временем становится кастрационно-резистентной как эволюционный ответ на АДТ. На этом этапе опухоли часто вновь становятся более ПСМА-авидными, что снова делает их подходящей мишенью для радиолигандной терапии. Это происходит потому, что ген ПСМА FOLH1 остаётся гиперэкспрессированным даже без участия сигнального пути AR. Таким образом, повышение уровня ПСМА по сути является побочным продуктом адаптивных механизмов, позволяющих раковым клеткам выживать под давлением терапии. Резистентные клетки, преодолевшие андрогенную депривацию, начинают размножаться и распространяться, что в конечном итоге делает АДТ неэффективной.
В таких случаях стандартным подходом является назначение ингибиторов сигнального пути андрогенного рецептора (ARPI), хотя их эффективность ограничена, так как андрогенный рецептор больше не является основным драйвером роста опухоли. Однако повышение уровня ПСМА при этом сохраняется — и именно эту уязвимость мы можем использовать.
Новая парадигма: комбинация подавления AR-пути с радиолигандной терапией (РЛТ)
Именно это и исследуют недавние клинические исследования: раннее выявление и таргетирование тех адаптивных раковых клеток, которые выживают после АДТ — что в перспективе позволяет подавить механизмы ускользания опухоли. Результаты обнадёживают: у многих пациентов вскоре после начала блокады AR наблюдается значительное повышение экспрессии ПСМА, что потенциально превращает пациента с «низкой экспрессией ПСМА» в кандидата на РЛТ.
Недавнее подтверждение этой концепции на начальных, гормоночувствительных стадиях было представлено на ASCO 2025: первые результаты испытания PSMAddition, где комбинация РЛТ и АДТ показала лучшие результаты по сравнению с монотерапией АДТ.
Эта синергия между гормональной блокадой и таргетированием ПСМА может ознаменовать новую главу в персонализированной терапии РПЖ и перенести её применение на самые ранние стадии заболевания.
Наш клинический опыт
В нашей клинике мы применяем эту концепцию на практике на протяжении многих лет. Мы успешно используем первоначальную антиандрогенную терапию у отобранных пациентов для стимуляции экспрессии ПСМА перед запланированной радиолигандной терапией — с отличными результатами. Этот подготовительный этап может изменить правила игры для пациентов с гетерогенной или низкой экспрессией ПСМА, выявленной при первоначальном ПСМА-ПЭТ стадировании.
В заключение:
- Низкая экспрессия ПСМА не является необратимой.
- Подавление андрогенного сигнального пути (путём снижения уровня тестостерона или через блокаду АR) способно вызывать повышение экспрессии ПСМА.
- Это открывает новые возможности для ранней РЛТ — даже у пациентов, изначально признанных неподходящими.
- Сочетание таргетных терапий, направленных на AR и ПСМА, может обеспечить дополняющие и потенциально синергетические преимущества в лечении.
По мере совершенствования стратегий лечения взаимодействие между гормональной манипуляцией и молекулярной ядерной терапией становится мощным инструментом в борьбе с раком простаты.
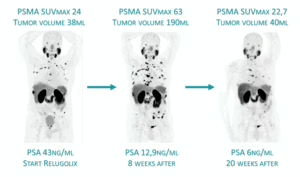
Сравнительные ПСМА-ПЭТ сканы у пациента, недавно начавшего АДТ, демонстрирующие выраженную гиперэкспрессию ПСМА через 8 недель, несмотря на значительное снижение уровня ПСА (псевдопрогрессия объема ПСМА и истинное прогрессирование накопления ПСМА на ПСМА-ПЭТ).